Control de Biofilms en las Industrias Alimenticia y Farmacéutica: Claves Técnicas y Lecciones del Webinar Hixwer–Christeyns
Los biofilms representan uno de los desafíos microbiológicos más importantes para las industrias alimenticia y farmacéutica. El 13 de noviembre, durante un webinar técnico organizado por Hixwer Argentina S.A., distribuidor exclusivo en Argentina de Christeyns, junto a Christeyns, la especialista Lizzie Rojas —Directora de Ventas en Chile, Christeyns— profundizó en los mecanismos que explican por qué los biofilms son tan resistentes y qué estrategias deben aplicarse para controlarlos de manera efectiva.
Quienes deseen ver la grabación completa del encuentro pueden registrarse aquí: https://www.hixwer.com/acceso-a-videos-seminario-deteccion-y-remocion-de-biofilms/
Qué es realmente un biofilm y por qué es tan difícil eliminarlo
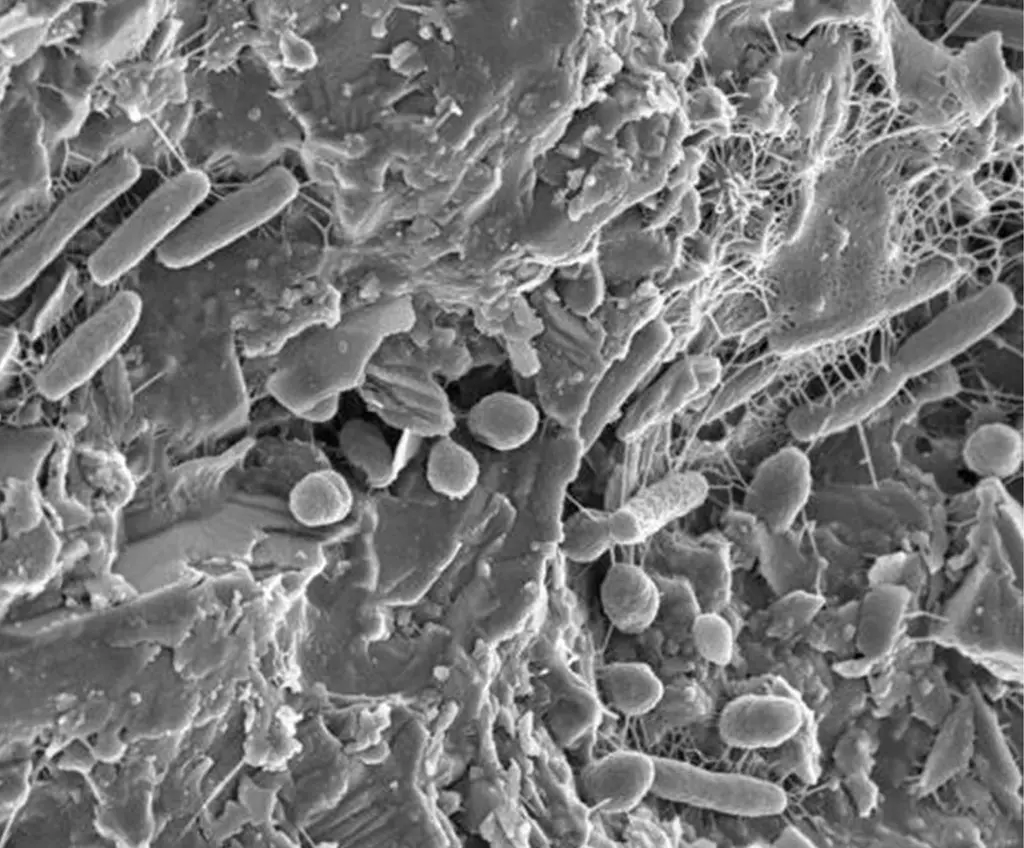
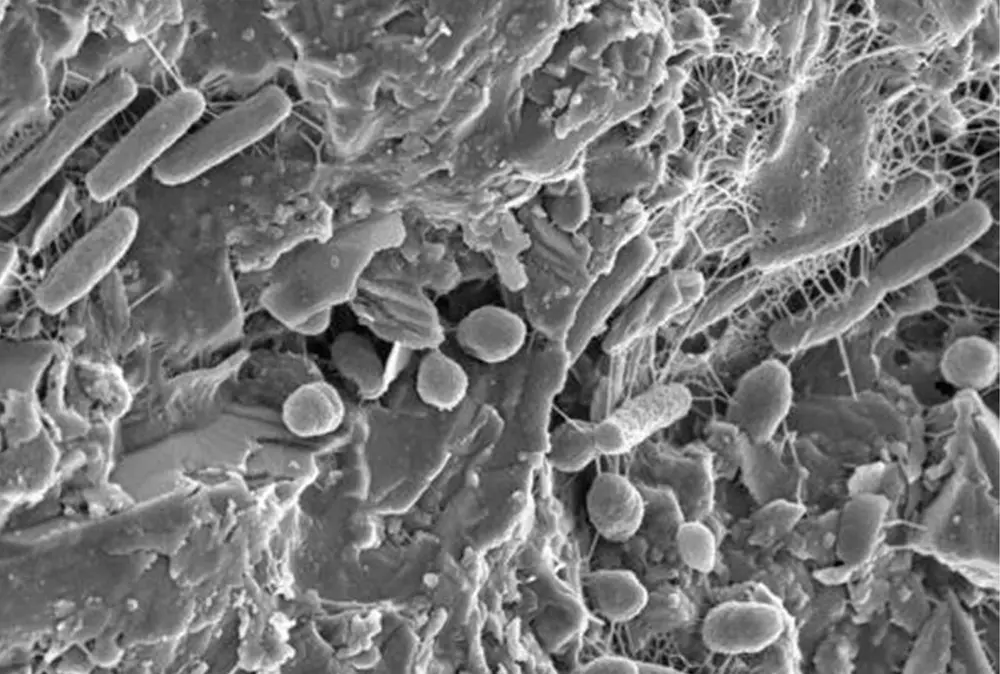
Fotografía de un biofilm bacteriano. Université catholique de Lovuvain. https://uclouvain.be/en/sciencetoday/news/les-biofilms-bacteriens-au-microscope.html
Según expuso Lizzie Rojas, un biofilm es “un caso particular de contaminación microbiológica formado por una comunidad de microorganismos embebidos en una matriz generada por ellos mismos”. Esa matriz —conocida como EPS— incluye polisacáridos, proteínas, lípidos, minerales, ADN y agua, creando un entorno estable y protector.
A diferencia de las bacterias en estado libre (planctónico), las células dentro de un biofilm:
- se adhieren fuertemente a superficies,
- se comunican entre sí mediante quorum sensing,
- se protegen de agentes externos,
- y desarrollan resistencia a desinfectantes y condiciones adversas.
Esta “vida comunitaria” les permite sobrevivir donde un microorganismo aislado no podría hacerlo.
Cómo se forma un biofilm: velocidad, etapas y el rol de la superficie
Uno de los puntos más críticos del webinar fue el énfasis en la velocidad de formación. Según Rojas, “en apenas 20 minutos una bacteria como Listeria monocytogenes puede comenzar su adhesión a superficies de acero inoxidable o goma”.
Si el proceso de higienización no es adecuado, en 24 horas el biofilm ya está formado y con una resistencia significativamente mayor.
El proceso ocurre en cuatro etapas:
- Adhesión: las bacterias encuentran una superficie con humedad, nutrientes y temperatura adecuada.
- Colonización: comienzan a agruparse y producir matriz extracelular.
- Maduración: se organizan en estructuras complejas con canales de agua.
- Dispersión: fragmentos del biofilm se desprenden y colonizan nuevas áreas.
De esta secuencia se desprende la principal conclusión operativa:
El mejor momento para actuar es en las primeras dos etapas, antes de que la estructura se consolide.
Superficies críticas y diseño higiénico: cuando el problema no es la bacteria, sino la planta
El webinar remarcó que prácticamente cualquier superficie puede servir como soporte para biofilms, pero algunas son especialmente favorables.
Materiales como el acero inoxidable 304 o 316 son estándar en la industria por su resistencia y limpiabilidad. Sin embargo, como advirtió Rojas, “el uso de elementos abrasivos genera microabrasiones imperceptibles, transformando una superficie higiénica en un refugio ideal para bacterias”.
También se destacó el impacto del diseño higiénico de equipos:
- zonas muertas,
- soldaduras deficientes,
- uniones difíciles de alcanzar,
- caños y circuitos CIP sin acceso visual,
- pendientes inadecuadas,
- o acumulación de humedad.
Todos estos factores generan nichos donde los biofilms se desarrollan sin ser detectados.
La contaminación recurrente muchas veces es consecuencia de estas fallas estructurales más que de un error de proceso.
Biofilms como reservorio de patógenos: el caso crítico de Listeria monocytogenes
La presentación dedicó un capítulo especial a Listeria monocytogenes, un patógeno de alto impacto en seguridad alimentaria. Aunque no requiere desinfectantes especiales, su capacidad de persistir en plantas durante meses o años se debe a:
- supervivencia a procesos incompletos de desinfección,
- exposición repetida a concentraciones subletales de químicos,
- refugio en biofilms ya formados,
- y fallas de limpieza en superficies poco accesibles.
Rojas remarcó que “no todas las cepas de Listeria son persistentes, pero algunas logran establecerse y reaparecer intermitentemente, generando falsos negativos y sorpresas en auditorías”.
La única estrategia efectiva es combinar prevención, detección y eliminación de biofilms, actuando tanto sobre el entorno como sobre los procesos.
Métodos de detección: por qué el ATP y el recuento tradicional no alcanzan
Los métodos más utilizados en planta —cultivo en superficie, ATP, hisopados rutinarios— son poco eficaces para anticipar la formación de un biofilm:
- tardan demasiado (más de 24–48 h en obtener resultados),
- no detectan estructuras tempranas,
- y no distinguen entre suciedad y biofilm incipiente.
Cuando el biofilm ya aparece en estos métodos, normalmente está demasiado avanzado.
Por eso la prioridad operativa es evitar que se formen, mediante:
- protocolos de limpieza sólidos,
- acción mecánica constante,
- verificación de cobertura,
- y revisión del diseño higiénico.
Control y eliminación: acciones prácticas para la industria
El webinar destacó cuatro pilares para reducir la incidencia de biofilms y su reaparición:
- Higiene mecánica intensiva en las primeras 24–48 h
Los biofilms jóvenes sí pueden ser removidos mediante fricción y detergencia adecuada.
- Evitar exposiciones subletales a desinfectantes
Concentraciones bajas favorecen la aparición de cepas adaptadas.
- Revisión del diseño higiénico
Zonas inaccesibles son caldo de cultivo para recurrencia.
- Programas específicos para patógenos persistentes
Especialmente en plantas con antecedentes de Listeria.
El rol de Hixwer: soluciones para un control eficaz del muestreo y la higiene
Durante la apertura del webinar, el equipo de Hixwer recordó que la prevención efectiva de biofilms comienza con una buena toma de muestras, realizada con insumos adecuados y con un protocolo consistente.
Las soluciones de muestreo de Hixwer —incluyendo bolsas estériles, dispositivos Sampling Systems y consumibles microbiológicos— permiten asegurar que cada etapa del proceso analítico preserve la integridad de las muestras y ayude a detectar problemas reales a tiempo.
La combinación de:
- equipos de muestreo seguros,
- protocolos de higiene adecuados,
- diseño higiénico,
- y productos específicos de limpieza y desinfección
Es lo que permite cerrar el círculo del control de biofilms en la industria.
Conclusión
Los biofilms no son un problema nuevo, pero sí uno que evoluciona con rapidez y exige un enfoque técnico sólido. Las industrias alimentaria y farmacéutica necesitan comprender cómo se forman, cómo detectarlos tempranamente y cómo actuar antes de que se conviertan en estructuras resistentes.
Como quedó claro en el webinar Hixwer–Christeyns, el control exitoso combina ciencia microbiológica, diseño higiénico y una estrategia integral de limpieza y muestreo.
Desde Hixwer, nuestro compromiso es acompañar a las plantas con tecnología, insumos confiables y capacitación, para que cada proceso sea más seguro, robusto y predecible.

Benito Lynch 479. Troncos del Talar, Buenos Aires, Argentina
Tel: +54 11 7078-6666
WhatsApp: +54 9 11 5696 2772
info@hixwer.com
https://www.hixwer.com/