
Análisis de Impurezas Elementales vía ICP Óptico y Masa

PARA CUMPLIR CON USP232/233/2232
Introducción
La detección de trazas de impurezas elementales en productos farmacéuticos es de altísima importancia, no solo por su toxicidad intrínseca, si no también porque deterioran las estabilidad y eficacia del medicamento. Las normativas USP 232/233 entraron en vigencia el 1° de enero de 2018, y regulan la cantidad máxima permitida de 15 impurezas elementales en productos farmacéuticos (incluido API’s) y cómo analizarlos. De estos elementos, es obligatorio analizar Cadmio, Plomo, Arsénico y Mercurio. Además, se encuentra armonizada con la farmacopea Europea, por lo cual será imperioso cumplir con estas regulaciones para toda la industria farmacéutica. Por otra parte, es la FDA quien tiene la potestad de implementar los controles y/o exigir que cumpla cualquier producto medicinal que ingrese a Estados Unidos.
En esta publicación, se presentarán datos concretos sobre como cumplir con la normativa USP 232 / 233 /2322 utilizando el ICP Óptico iCAP 7600 y el ICP – Masa iCAP TQ de Thermo Scientific.
Análisis via ICP Óptico
Instrumentación
El iCAP 7600 DUO de Thermo Scientific es el ICP – OES de mayor performance para cumplir con USP232/233, gracias a su bajo límite de detección para los analitos de interés y la posibilidad de resolver espectros de emisión complejos (por ejemplo en presencia de elementos como Pt, Pd e Ir) con el software Qtegra ISDS. Además, el asistente Element Finder para desarrollo de métodos provee una interfaz intuitiva, seleccionando elementos desde una tabla periódica virtual que automáticamente elige las líneas de emisión sin interferencias. Adicionalmente se encuentran disponibles Kits de validación y soporte completo para 21 CFR Part 11.
Preparación de muestras y patrones
Se seleccionaron para este estudio dos medicamentos de venta libre: un Anti- inflamatorio (Drug 1) y un Anti – histamínico (Drug 2). Todas las muestras se prepararon disolviendo 0.5 g del medicamento en 20g de Dimetil Sulfóxido (DMSO) de Pureza ≥99.8% (Fisher Scienticific), y sonicando por 10 minutos. Luego se agrego más DMSO hasta obtener 25 g de solución. Debido a su alto punto ebullición, muestras preparadas en este solvente se pueden correr con el Kit de introducción de muestras acuosas, con la precaución de cambiar las mangueras de PVC por Siliconadas.
Los patrones se prepararon a partir de soluciones monoelementales de 1000 mg/ L (Fisher Scientific) en las concentraciones esperadas para los elementos de interés.
El análisis se llevo a cabo de acuerdo a lo estipulado por la USP 233: En primera instancia se preparon tres patrones en DMSO puro a concentraciones 0 J, 0.5 J y 2.0 J para los analitos de interés. La Tabla 1 indica los Target Limits J calculados con la PDE (Dosis Diaria Permitida) del elemento y la dosis máxima del medicamente (2 g en ambos casos). Luego, se prepararon las muestras de los medicamentos con un fortificado (spiking) a valores 0.5J y 1.5 J; y un conjunto de seis muestras independientes fortificadas a 1.0 J para el test de Precisión. Finalmente, para demostrar la ausencia de deriva, se analizó el patrón de 2.0 J al final de la corrida.
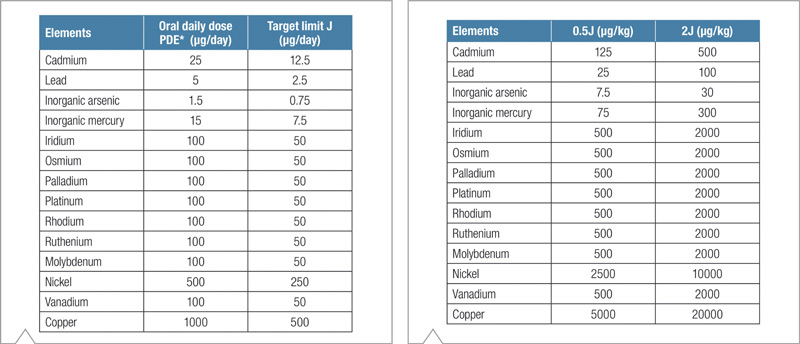
Tabla 1. Target Limits (J) para 14 elementos especificados en la norma USP<232>, por ingesta oral PDE. No se analizó Cromo ya que no se sospechaba su inclusion en el medicamento.
Tabla 2. Patrones de Calibración usados para el análisis, teniendo en cuanta la dilución 1:50 de la muestras (en ppb).
Desarrollo de Método
Las longitudes de onda para los analitos de interés se seleccionaron en base a la intensidad relativa y potenciales interferencias. Para optimizar el instrumento, se analizó una muestra fortificada con los elementos de interés con la función Optimize Source del software Qtegra ISDS. Esta rutina determinó las condiciones óptimas del plasma e introducción de muestra, para obtener la mejor sensibilidad (Tabla 3). En las figuras 1 y 2 se muestran Curvas de calibración representativas para Pb e Ir.
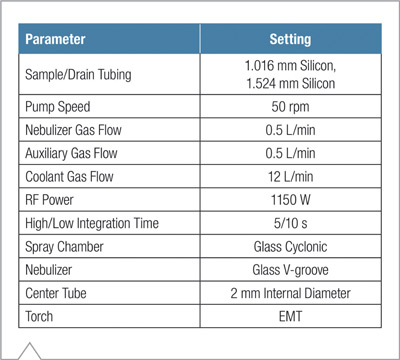
Tabla 3. Introducción de muestra y Parámetros del plasma usados durante el análisis.
Los límites de detección del método (MDL) se calcularon para todos los elementos y se presentan en la Tabla 4. En todos los casos son al menos 1 orden de magnitud más pequeños que el valor J (Target Limit).
Las concentraciones medidas para cada analito (con tres repeticiones) para ambos medicamentos, se encuentran por encima del límite de detección, como se muestra en la Tabla 5.
Resultados y Analisis de los datos
La deriva (drift) del instrumento se determinó comparando los resultados obtenidos al medir el patrón de 2 J antes y luego de las muestras. Los resultados que se presentan en la tabla 6 cumplen el criterio de aceptación (< 20%) para cada elemento. Como parte de la validación, la exactitud se midió de acuerdo a lo requerido por la USP233, midiendo los Recoveries (recuperos) de las muestras fortificadas a valores 0.5 J y 1.5 J. Los valores se presentan en la Figuras 3 y 4, siendo los límites aceptados entre 70% y 150% para la media de tres mediciones, que el iCAP 7600 cumple sin problemas.
La precisión se determinó analizando 6 muestras individuales del material fortificado con los elementos de interés, a la concentración J. El Criterio de aceptación estipula que la desviación estandar no debería exceder el 20%: el iCAP 7600 presenta un valor de 1% . Los resultados se muestran en la Tabla 7 para el Medicamento 1 y en la Tabla 8 para el Medicamento 2, en ambos casos cumplen con la regulación. La Robustez del método se determinó volviendo a correr las muestras, en el mismo instrumento, un día después. El criterio para pasar este test es una RSD% menor a 25% entre los valores, que el iCAP 7600 cumple.
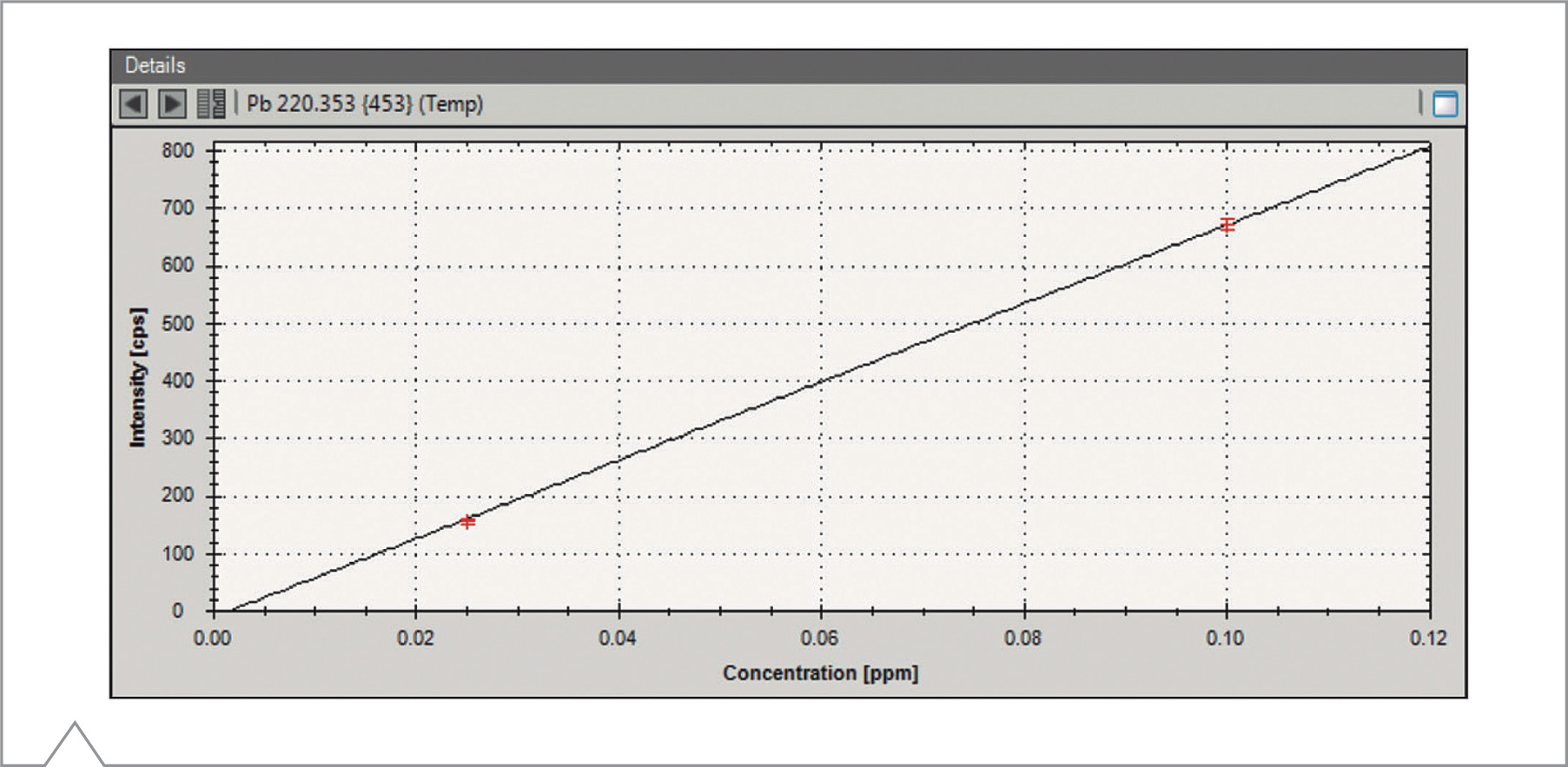
Figura 1. Curva de Calibración para Pb usando la línea de emisión a 220.353 nm, medida a 0J, 0.5J y 2J
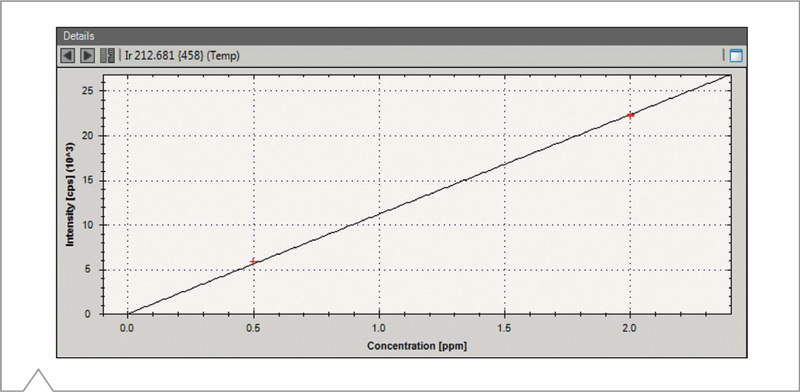
Figura 2. Curva de Calibración para Ir usando la línea de emisión a 212.681 nm medida a 0J, 0.5J y 2J.
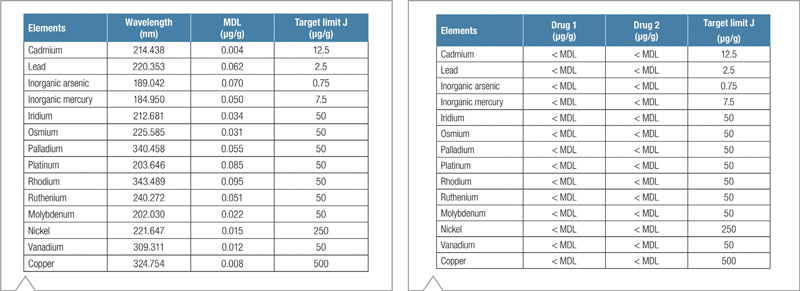
Tabla 4. Límites de Detección del Método para los medicamentos estudiados, comparados con el valor J.
Tabla 5. La Tabla muestra que la concentración para cada analito de interés se encuentra por encima del Límite de Detección del Método.
Análisis via ICP Masa
Instrumentación
Todas las mediciones se realizaron en un ICP Masa Triple Cuadrupolo modelo iCAP TQ de Thermo Scientific. La operación se realizó integramente desde el software Qtegra ISDS y se calibró a diario con una solución patrón. Los parámetros típicos de operación se muestran en la Tabla 9.
Desarrollo de Método
La técnica de ICP – MS no se encuentra exenta de interferencias, pero con los recientes desarrollos, hay formas de minimizarlas mediante la formación de nuevas especies en la celda de colision/reacción. Para seleccionar los parámetros óptimos para la corrida analítica, se utilizó el asistente Reaction Finder del software Qtegra. Este poderoso y completo asistente permite armar un método de análisis para todos los elementos de interés sin conocimiento previo o detallado de ICP – MS por parte del usuario. En el presente trabajo, seleccionó O2 para el análisis de As en modo Triple Cuadrupolo (TQ) y Simple Cuadrupolo (SQ – KED) para Cd, Hg y Pb. Bajo estas condiciones, el As se analiza en m/z 91, mientras que el resto se analiza en el mismo modo que lo haría un ICP – MS de Cuadropolo Simple.
Preparación de muestras y patrones
En este caso, se eligió la Vitamina B12 (Cianocobalamina) para demostrar el flujo de trabajo para USP 232/233, que también aplica para Suplementos Dietarios, bajo la normativa USP 2232. Esta vitamina juega un rol fundamental en el sistema nervioso y se encuentra disponible en muchos medicamentos y suplementos de venta libre, algunos con hasta 5 mg de esta sustancia.
Debido a la cantidad de Cobalto presente en la vitamina (cerca del 3% de la masa), aparece una interferencia poliatómica importante para la determinación de As: la formación de 59Co16O+ de 75 amu, ya que el Arsénico tiene únicamente un isótopo con esa masa atómica. Sin embargo, utilizando O2 como gas de reacción, la masa del analito aparece ahora en 91 amu, por la formación de la especie 75As16O+.
Para preparar las muestras, se tomaron 10 mg de la Vitamina B12 pura y se disolvieron en 10 mL de HNO3 1% para un factor de dilución 1000. Esta solución se volvió a diluir antes de la medición final. Además, se preparó una muestra de un suplemento con Vitamina B12, soluble en agua, que se preparó de acuerdo a las indicaciones del productor: en una botella se mezclaron 500 mg del suplemento 7 mL de agua, 1 mL de HCl concentrado para estabilizar el Hg, y luego se agrego Ácido Nítrico 1% para llevar a un volumen de 100 mL.
Una solución de estandar interno se agregó a todos los viales manualmente, de forma tal que tanto blanco, patrones y muestra contengan 1 ng/mL de Itrio y Bismuto. En una segunda preparación, se agregó Butanol a todos los blancos, patrones y muestras para minimizar las diferencias entre el contenido de Carbono entre muestras; y mitigar el efecto de ionización más eficiente para As y Se.
En el presente estudio, solo se analizaron cuantitavamente los cuatro elementos obligatorios según USP 232: As, Cd, Pb y Hg. Las otras impurezas elementales (por ejemplo catalizadores comunes, como Ir, Pd, Ru, Rh) se determinaron cualitativamente con un análisis completo de masas. Como parte de un análisis de riesgo, estos elementos pueden omitirse del análisis cuantitativo y reducir la carga de trabajo, pero analizarse en caso que no pasen el test cualitativo.
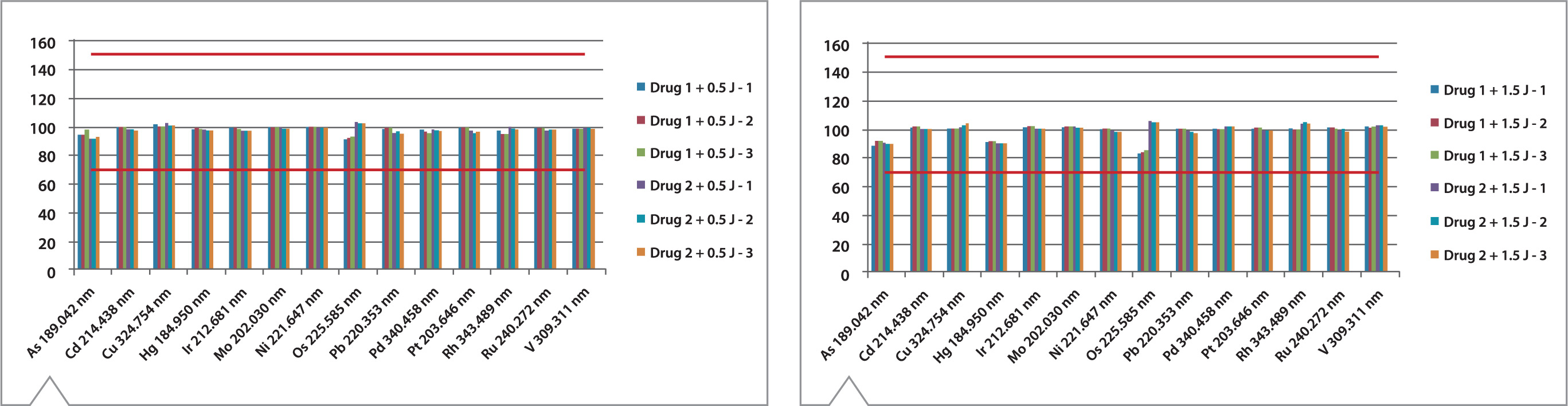
Figura 3. Recoveries para el fortificado a 0.5J. Las líneas rojas demarcan los límites de 70% y 150%.
Figura 4. Recoveries para el fortificado a 1.5J. Las líneas rojas demarcan los límites de 70% y 150%.
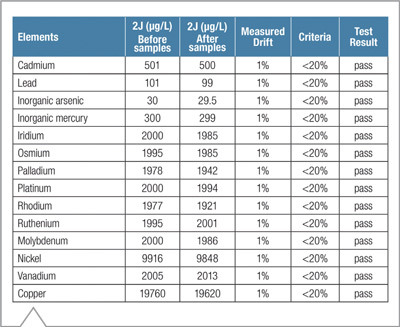
Tabla 6. Comparación de las concentraciones medidas para el Patrón de 2 J, medido antes y después de las muestras. La variación (drift) es del 1%, muy por debajo del límite de aceptación de 20%.
Resultados y Analisis de los datos
De acuerdo a lo regulado por la normativa USP 2232, el producto cumple si el nivel de impurezas elementales no excede los valores mencionados en la Tabla 10. Usando un instrumento de Simple Cuadrupolo, el Arsénico se suele analizar en modo KED (Kinetic Energy Discrimination) para suprimir la interferencia poliatómica 40Ar35Cl+. Sin embargo el análisis de la Vitamina B12 pura muestra diferencias notables mediante el modo Simple y Triple cuadrupolo, como puede verse en la Tabla 11. Esto es debido a que el ión 59Co16O+ no puede suprimirse completamente en modo Simple Cuadrupolo, generando un falso positivo para el blanco de As, y por lo tanto un mayor BEC que hace que el producto no pase los tests de USP. En cambio en modo TQ, esta interferencia desaparece y se obtiene un Recovery completo de las muestras fortificadas con As, cumpliendo así con la normativa. Además, el modo TQ incrementa la sensibilidad para As, como puede verse en la Figura 5.
En cuanto al Suplemento dietario, para validar la exactitud, se analizó un conjunto de muestras con y sin fortificado (a nivel 0.5 J), los resultados se muestran en la Tabla 12. Debido a la baja concentración de Vitamina en el producto, este pasa el test de USP, pero la concentración de Arsénico determinada es 10 veces mayor mediante modo SQ que por TQ.
Por otra parte, los Recoveries obtenidos son buenos excepto para As. Como se mencionó antes, esto puede mitigarse mediante el agregado de un solvente orgánico miscible. La anomalía se debe al cambio en la eficiencia de ionización del As, por parte de compuestos carbonados presentes en el suplemento dietario, por ejemplo aminoácidos. La última columna de la Tabla 12 confirma esto: se corrieron las muestras nuevamente, agregando 1% v/v de Butanol, para tener un Carbon Matching en la eficiencia de ionización.
Finalmente, la Tabla 13 presenta los resultados de Límite de Detección del Instrumento (IDL) y Límite de Detección del Método (MDL). Este último es más conservador en cuanto a la mínima cantidad que puede ser detectada ya que depende de la composición de las soluciones y los pasos llevados a cabo.
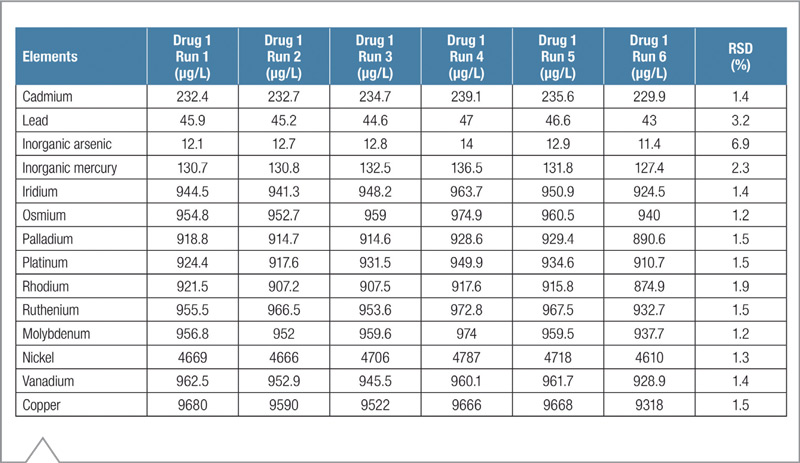
Tabla 7. Concentraciones medidas para seis repeticiones del Medicamento 1 fortificadas a 1 J.
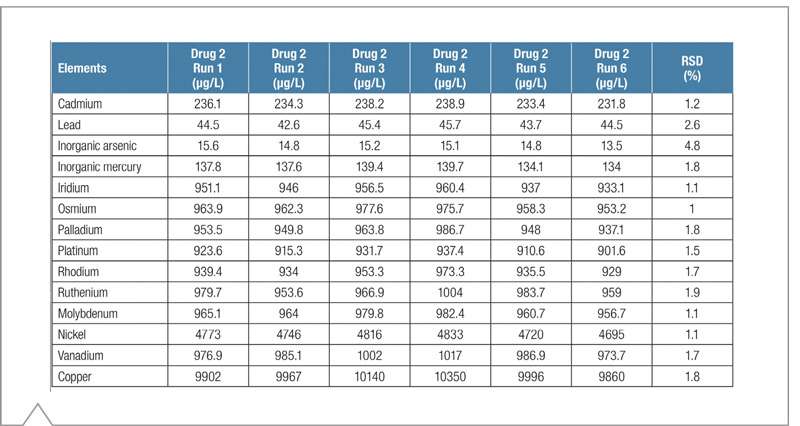
Tabla 8. Concentraciones medidas para seis repeticiones del Medicamento 2 fortificadas a 1 J.
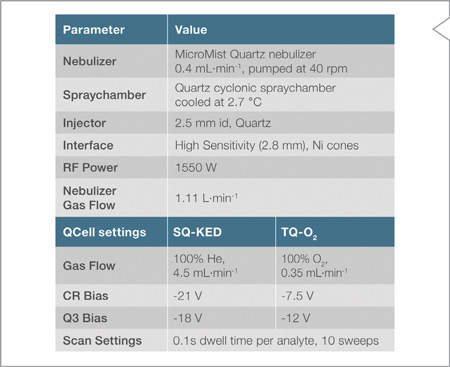
Tabla 9. Parámetros típicos del iCAP TQ para una corrida analítica.
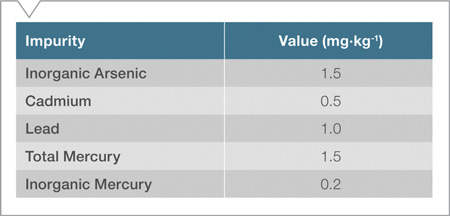
Tabla 10. Límites aplicables para suplementos dietarios, para una dosis diaria máxima de 10g.
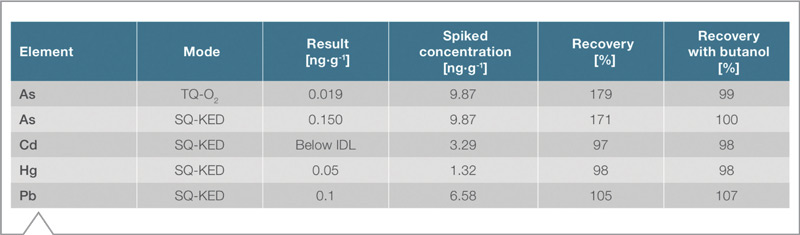
Tabla 11. Comparación de los modos SQ – KED y TQ – O2 para Arsénico en la muestra de Vitamina B12.
Tabla 12. Resultados para el Suplemento Dietario con Vitamina B12.
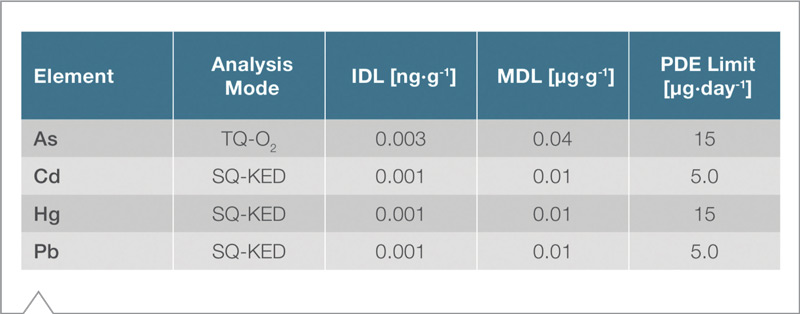
Tabla 13. Comparación de los Límites de Detección Instrumentales (IDL), Límites de Detección de Método(MDL), y el PDE.
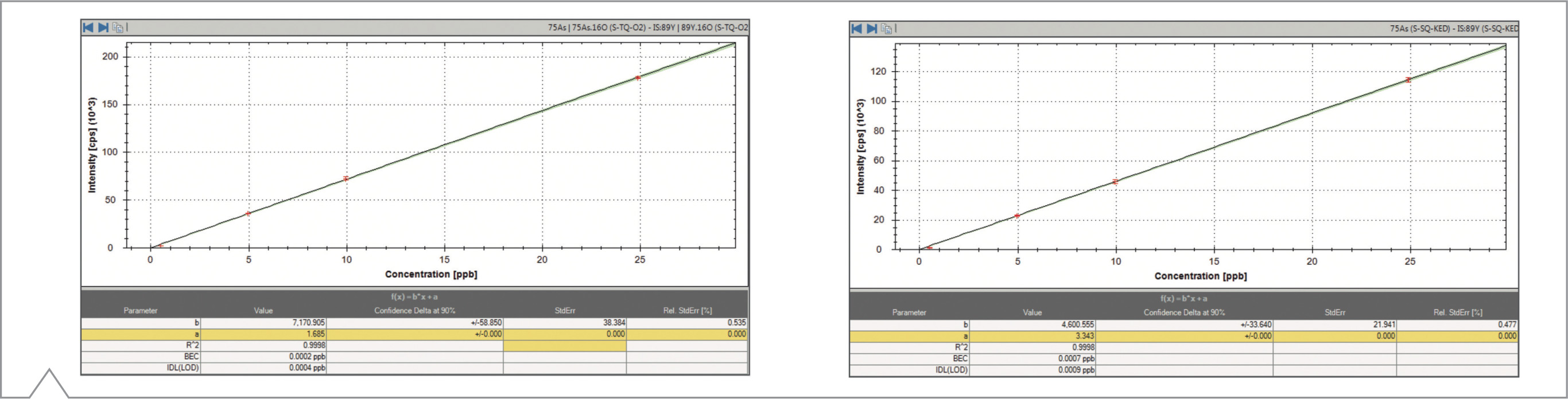
Figura 5. Curvas de calibración para As en ambos modos: TQ – O2 (izquierda) y SQ – KED (derecha).
Conclusión
En el presente trabajo se presentaron datos concretos sobre la implementación de las Técnicas Espectroscópicas de ICP Óptico e ICP Masa para cumplir con las normativas de USP232/233/2232. Utilizando los Instrumentos de Thermo Scientific, se obtienen excelentes resultados a la vez que el método puede implementarse fácilmente con el software Qtegra.
Soluciones Analíticas S.A. (representante autorizado de Thermo Scientific) le ofrece todo lo necesario para implementar y cumplir con USP232/233/2232.


















