
Cuando HPLC no es la solución: Análisis por Cromatografía Iónica Metrohm

Cuando HPLC no es la solución: Análisis por Cromatografía Iónica Metrohm
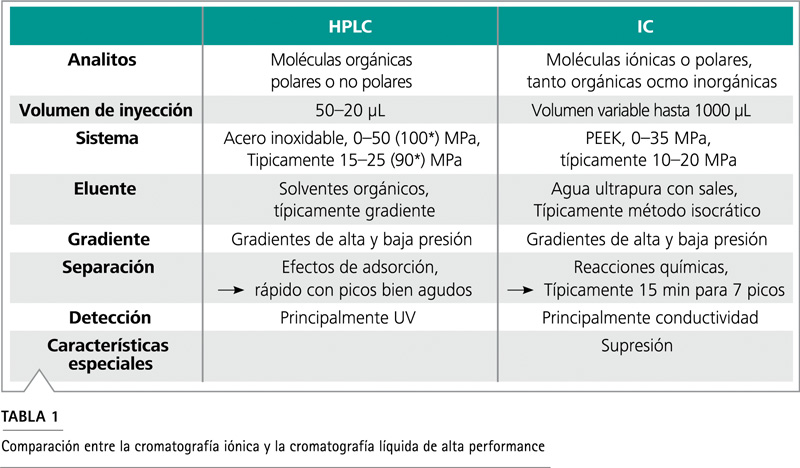
La cromatografía líquida de alta eficacia (HPLC, por sus siglas en inglés) y la cromatografía iónica (IC, por sus siglas en inglés) son comúnmente usadas en el sector farmacéutico, alimenticio y ambiental para analizar componentes específicos en muestras y para verificar el cumplimiento de normas y estándares. Sin embargo, los usuarios de HPLC pueden encontrarse con las limitaciones propias de esta técnica, por ejemplo, cuando se analizan aniones estándar o ciertas impurezas farmacéuticas. Este documento técnico describe cómo tales desafíos pueden superarse con IC.
¿Qué es la cromatografía líquida?
El término cromatografía líquida (LC, por sus siglas en inglés) hace referencia a una clase de técnica fisicoquímica para separar y cuantificar compuestos en una muestra. La LC involucra una fase móvil, la cual eluye la muestra, y una fase estacionaria donde toma lugar la separación. La fase estacionaria consiste de pequeñas partículas en el rango de los µm empacadas en una columna.
La separación de los compuestos de la muestra está basada en la fuerza relativa de interacción con la fase móvil y la fase estacionaria: compuestos con una gran afinidad por la fase estacionaria van a experimentar una retención más fuerte en la columna y, por lo tanto, van a eluir después de compuestos con una afinidad relativamente menor con la fase móvil. Siguiendo con la separación, los compuestos pueden ser cuantificados usando una variedad de diferentes técnicas de detección. La cromatografía iónica (IC) y la cromatografía de alta eficacia (HPLC) se encuentran entre las cromatografías líquidas más comúnmente usadas en la química analítica. Para varias industrias son herramientas esenciales, las cuales son usadas desde la inspección de materias primas hasta el análisis de aditivos en el control de calidad del producto final. Incluso hasta muestras sensibles a la temperatura pueden ser analizadas sin ningún problema, ya que ambas técnicas pueden ser llevadas a cabo a temperatura ambiente.
La LC se ha vuelto indispensable en la producción farmacéutica como también en la alimenticia, en la de bebidas y en el análisis de agua – desde aguas ambientales hasta aguas de proceso o residuales. En estos sectores fuertemente regulados, IC y HPLC proveen análisis sensibles y selectivos que aseguran el cumplimiento de normas y estándares.
HPLC vs. IC: Las diferencias
En la literatura la diferencia entre HPLC e IC no es clara. De hecho, las dos técnicas están estrechamente relacionadas. Por lo tanto, ¿cuáles son las diferencias entre HPLC e IC?
Mecanismos de separación
En HPLC, la separación está basada en interacciones hidrofílicas (HPLC de fase normal) o en interacciones hidrofóbicas (HPLC de fase reversa) de los analitos con la fase estacionaria. Esto ocasiona que la técnica sea adecuada para la separación de compuestos orgánicos polares o no polares. El HPLC de fase reversa es el modo más usado de HPLC con la mayor cantidad de aplicaciones. La separación recae sobre los solventes orgánicos que son usados como eluentes.
En IC, el mecanismo más importante de separación es el intercambio de iones. Otros mecanismos, como exclusión y partición iónica también son usados, dependiendo de la aplicación. La separación por intercambio iónico recae en las reacciones químicas de los analitos iónicos con los grupos de intercambio iónico de la fase estacionaria, a diferencia de las interacciones físicas como en HPLC. Sin embargo, la separación de compuestos polares no-iónicos es igualmente posible usando equipos para IC, eligiendo correctamente la columna y la fase móvil usadas. Esto ocasiona que la IC sea apropiada para la separación de iones orgánicos e inorgánicos y de sustancias polares.
Eluentes
Las separaciones por HPLC son realizadas usando solventes orgánicos como eluentes, utilizando generalmente gradiente de elución para obtener buena resolución para los analitos débilmente retenidos y apresurar la elución de los analitos fuertemente retenidos. Para poder ser miscibles con el eluente, las muestras son típicamente disueltas en solventes orgánicos. A diferencia del HPLC, en la IC la separación toma lugar en la fase acuosa. Los eluentes típicos son hechos con agua ultrapura con sales o ácidos disueltos. La gran mayoría de las separaciones por IC pueden ser realizadas con una elución isocrática, es decir, sin un gradiente.
Columnas
Tanto en HPLC como en IC, las columnas están basadas en partículas modificadas en la superficie como fase estacionaria que interactúan con los analitos a ser separados. Pero la funcionalización de la superficie difiere: en IC, la fase estacionaria es caracterizada por grupos intercambiadores de cationes o aniones, mientras que el HPLC utiliza grupos funcionales hidrofóbicos (HPLC fase reversa) o polares (HPLC fase normal).

Detección
El detector primario usado en HPLC es un detector UV. El detector UV es capaz de determinar sustancias que absorben la luz: el eluyente que sale de la columna es irradiado con luz UV. El analito es cuantificado por la diferencia de absorción entre la fase móvil (sin la muestra) contra el eluente conteniendo al analito.
En IC, el detector más comúnmente usado es el de conductividad. Este detecta y cuantifica al analito midiendo los cambios de conductividad del eluato. La detección por conductividad es una técnica no selectiva, pero con una sensible detección.
Cuando el HPLC falla
Limitaciones del HPLC
Hay limitaciones en lo que el HPLC puede hacer, las cuales son principalmente debidas a las columnas y detectores usados. Por ejemplo, no es posible separar con las columnas de HPLC la mayoría de los analitos iónicos. Esto significa que el HPLC no es adecuado para el análisis de aniones estándar o cationes en agua y en varios alimentos. Lo mismo sucede para ácidos orgánicos en, por ejemplo, vino, cerveza, o productos diarios.
En otros casos, el HPLC puede alcanzar sus límites en el paso de detección: la detección UV requiere que el analito absorba luz UV. Ciertos analitos, que son importantes en el análisis de agua, alimentos y productos farmacéuticos, incluyendo fluoruro y cloruro, no absorben luz UV, por lo que no pueden ser determinados mediante HPLC.
Superando las limitaciones del HPLC usando IC
Cuando el HPLC falla, la cromatografía iónica suele usualmente proveer una solución. Usando el intercambio iónico como mecanismo de separación, la IC permite la separación de muchos analitos que no pueden ser saparados en columnas de HPLC. La IC es ideal para la separación y determinación de moléculas iónicas y polares, tanto orgánicas como inorgánicas.
Además, los analitos que no absorban luz UV, como fluoruro o cloruro, pueden ser determinados por IC gracias al detector de conductividad. Con el uso de un detector de conductividad con supresión, el cual será explicado en el siguiente apartado, una muy alta sensibilidad puede ser alcanzada.
Supresión
Supresión: incremente la sensibilidad de la medición
La separación por cromatografía iónica requiere buffers conductores en la fase móvil. Además, el eluato que sale de la columna es altamente conductivo. La detección de conductividad del analito iónico contra la alta conductividad del fondo no es ideal. La solución a este problema se llama supresión: la supresión baja la conductividad del fondo. Los análisis de cromatografía iónica, en particular de aniones, casi siempre involucran supresión.
Las sales de ácidos débilmente disociados, por ejemplo, carbonato de sodio o bicarbonato de sodio, son usados como eluentes en la cromatografía de intercambio iónico. Durante la supresión, los iones positivamente cargados del eluente son reemplazados por protones por intercambio iónico. El ácido carbónico formado como resultado está débilmente disociado y exhibe una conductividad residual muy baja. Asimismo, los contraiones cargados positivamente de los aniones del analito son reemplazados por protones. Como resultado, la conductividad del eluato conteniendo al analito se incrementa sustancialmente.
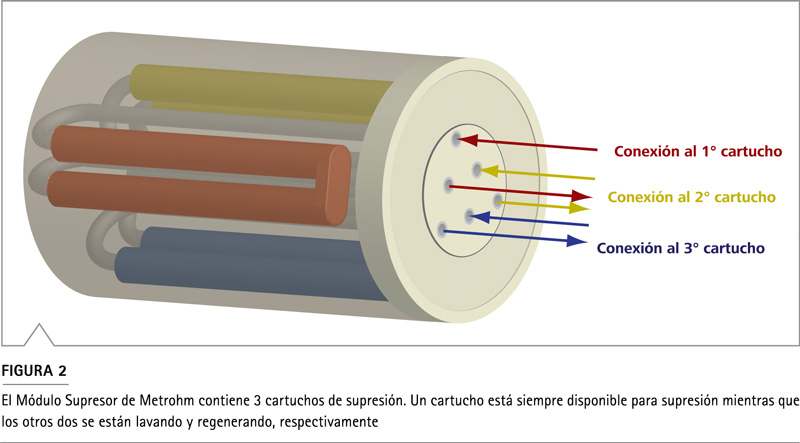
Para resumir, la supresión disminuye la conductividad de fondo del eluente, minimiza el ruido de la línea de base, optimiza la relación señal-ruido, e incrementa la sensibilidad del sistema de medición.
Ejemplo de aplicación: Aniones Inorgánicos en agua potable de acuerdo a EPA 300.1 partes A y B.
Alcance
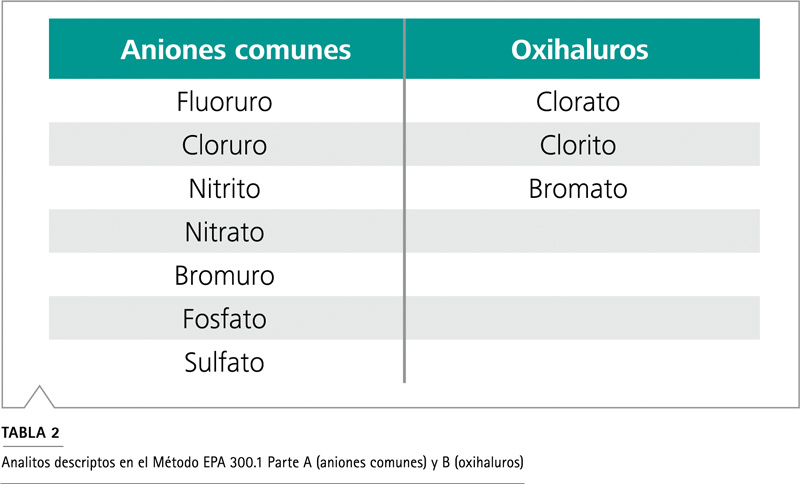
El Método EPA 300.1 describe la determinación de aniones inorgánicos en agua potable por cromatografía iónica. Los aniones cubiertos por la norma incluyen 7 aniones comunes (Parte A) y 3 oxihaluros (Parte B). Esto último ocurre al beber agua como subproductos de desinfección. Se pueden observar más detalles en la Tabla 2. Con IC, es posible determinar tanto aniones como oxihaluros en una simple corrida.
Resultados
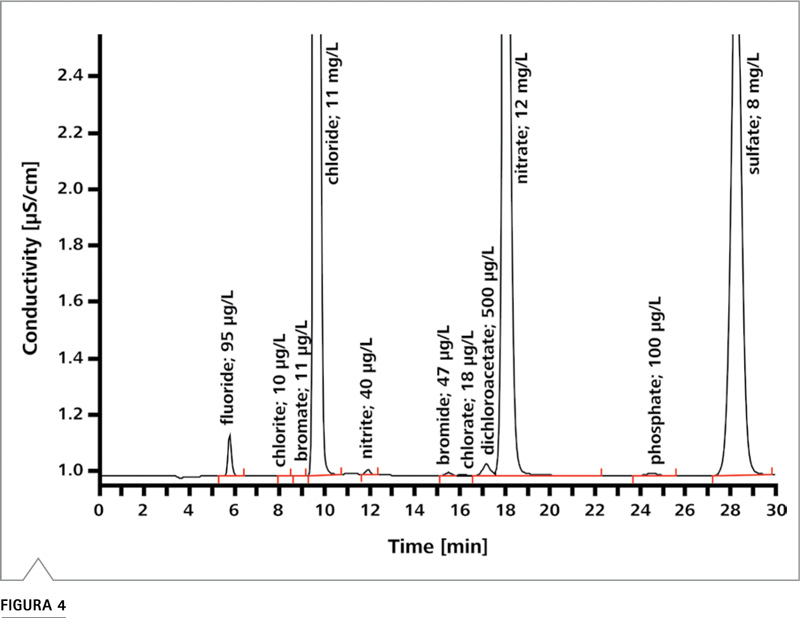
Mayor información
Para información más detallada sobre esta aplicación, puede visitar www.metrohm.com/applications y descargar la nota de aplicación AN-S-312.
Más aplicaciones en el campo de análisis de aguas pueden ser encontradas en nuestro catálogo <<Análisis de aguas>> disponible para ser descargado en www.metrohm.com/documents/80005141

















