Cultivo de células sin contaminación

Cuando se trabaja con los cultivos de células, la contaminación es un problema muy extendido. Para conseguir evitarla, es imprescindible mantener una buena esterilización en la técnica de trabajo y un manejo cuidadoso de los cultivos. Además, la incubadora de CO2 desempeña un papel importante, ya que ofrece unas condiciones de crecimiento ideales no solo para los cultivos de células, sino también para muchos microbios indeseados. Toda buena incubadora de gasificación ofrece numerosas prestaciones para evitar la contaminación. No obstante, para tomar una decisión sensata a la hora de adquirir una incubadora de CO2, no deben considerarse únicamente los aspectos técnicos. Más bien debe compararse y valorar los sistemas en su totalidad y, en particular, los conceptos de anticontaminación. En este caso concreto queda patente que los sistemas complejos no tienen por qué ser más seguros que los sencillos.
El equipo debe contribuir a evitar la contaminación de forma fiable, rápida y sencilla y sin elevados costes de consumibles.
Importancia del control de la contaminación en los trabajos con cultivos de células
La contaminación microbiana causada por bacterias, hongos o virus, representa un riesgo difícilmente calculable en el trabajo con cultivos de células. A menudo, las impurezas se descubren a posteriori, ya que no están necesariamente relacionadas con el crecimiento excesivo visible de las células cultivadas. Los efectos más sutiles como la modificación del valor del pH esencial de 7,4 para células humanas y células de mamíferos, se derivan de la privación de nutrientes importantes y la excreción de productos metabólicos microbianos, lo que supone el deterioro de la proliferación celular. Las temidas infecciones por micoplasmas pueden desencadenar cambios en la morfología de la célula huésped o incluso modificaciones genéticas, sin ser perceptibles de ninguna otra forma. Así, en casos extremos, un solo germen puede frustrar el trabajo de investigación de semanas o meses.
Existen muchas vías de propagación de la contaminación. Entre ellas se encuentra el uso de líneas celulares, medios, sueros u otros reactivos contaminados, y no detectados, por los gérmenes del aire, equipos insuficientemente desinfectados o incluso por la transmisión del personal de laboratorio. Dado que muchas veces puede ser costoso demostrar la ausencia de gérmenes, es preciso tomar medidas efectivas para controlar la contaminación.
Con los importantes avances en el campo de las aplicaciones de cultivos de células sensibles como, por ejemplo, la ingeniería de tejidos o la terapia regenerativa de células y tejidos, han aumentado los requisitos de higiene en las incubadoras de CO2. Actualmente se imponen estándares muy elevados de perfección y fiabilidad de todo el proceso, durante el cual la incubadora de CO2 asume un papel central. En el caso de todos los medicamentos terapéuticos basados en células como, por ejemplo, la suspensión celular de condrocitos autólogos, utilizada para la reimplantación en pacientes, se ha demostrado que es un problema que no sean esterilizables en sí. Así, la Directiva GMP1 (Buenas prácticas de fabricación), la Directiva GCCP2 (Buenas prácticas en cultivos de células) y la Directiva de la UE sobre la donación de células y tejidos3 recomiendan, entre otros, emplear artículos estériles de un solo uso o bien esterilizar los equipos reutilizables cuando se trabaje con células y tejidos humanos. En los cultivos de células deben garantizarse condiciones de esterilidad durante todo el tiempo que dure el cultivo. De lo contrario, no solo existe riesgo de propagación de la contaminación sino peligro de infección con riesgo para la vida del paciente.
Definición de términos: descontaminación, desinfección, esterilización
En primer lugar, deben explicarse los conceptos de uso frecuente: esterilización, descontaminación y desinfección.
Descontaminación es un término general que describe la eliminación de contaminantes peligrosos. La descontaminación abarca la contaminación biológica, química y radioactiva, pero no permite extraer conclusiones sobre su efectividad.
La desinfección desempeña un papel crucial en el método de trabajo aséptico del ámbito de la medicina. Se habla de desinfección cuando, en un procedimiento de prueba concreto, se alcanza una reducción de los gérmenes de cinco potencias de diez, esto es, que de los 100.000 gérmenes iniciales replicables sobrevive uno como máximo.
Poresterilización se entiende la eliminación completa de los microorganismos viables. Dado que, en la práctica, no es posible llevar a cabo una esterilización completa al cien por cien, diferentes farmacopeas establecen de forma unánime que, después de una esterilización efectiva, solo una de un millón de unidades esterilizadas puede contener un germen formador
de colonias. Con esta mínima posibilidad residual de que sobreviva un germen, la esterilización resulta más segura en comparación con la desinfección.
En relación con el funcionamiento y la comprobación de la efectividad de los métodos de desinfección y esterilización4, existen diferentes directivas y normas que se aplican especialmente en el sector farmacéutico y en el ámbito clínico. Las farmacopeas describen los métodos “clásicos” de esterilización mediante calor húmedo (autoclave), calor seco (esterilizador por aire caliente), fumigación con óxido de etileno y filtración estéril. La idoneidad de cada método depende del ámbito de aplicación específico y requiere su validación mediante el uso de determinados gérmenes indicadores.
Medidas para evitar la contaminación mediante incubadoras de CO2
El requisito de ambiente estéril para un cultivo celular vivo dentro de la incubadora de CO2 representa un desafío técnico que no debe subestimarse, ya que las condiciones óptimas de crecimiento en una incubadora favorecen al mismo tiempo la multiplicación de microorganismos no deseados.
En principio, en un concepto de control de contaminación para una incubadora de CO2 deben observarse los siguientes aspectos críticos:
- Idoneidad del interior de la incubadora para la desinfección periódica mediante pulverización/ limpieza, que representa un método importante y habitual para reducir el número total de gérmenes, es decir, la carga microbiana del sistema de la incubadora de CO2.
- Contar con un equipo para eliminar completamente los contaminantes potenciales mediante un procedimiento de esterilización sencillo y efectivo, capaz de suprimir el foco de contaminación a intervalos regulares o según sea necesario.
- Evitar el uso de estructuras como conductos de aire, ventiladores o bastidores para bandejas que puedan acumular contaminación. Su limpieza resulta costosa y, por ello, deben retirarse antes de llevar a cabo la esterilización.
- Evitar el agua de condensación como criadero de gérmenes en la sala de incubación, ya que los microbios solo se reproducen en lugares húmedos.
- Impedir la transmisión de gérmenes por el aire que están presentes en cierta medida en los trabajos en salas blancas.
Medidas para evitar la contaminación mediante incubadoras de CO2
Los fabricantes de incubadoras de CO2 han desarrollado prestaciones muy diferentes con procesos parcialmente complejos para evitar la contaminación, y se han adaptado a las necesidades de las incubadoras de CO2. Al respecto hay que diferenciar entre medidas de descontaminación, que pueden llevarse a cabo periódicamente o según necesidad, y que requieren la desconexión del equipo durante un tiempo determinado, y prestaciones con las que se trata de reducir constantemente la probabilidad de contaminación. En la tabla 1 se enumeran las medidas y procedimientos relacionados más habituales.
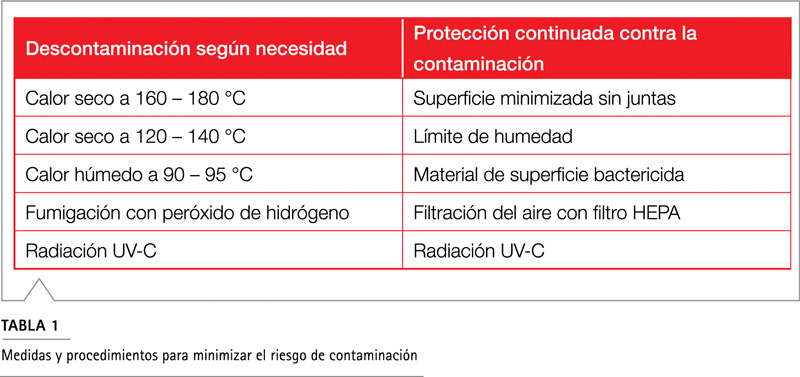
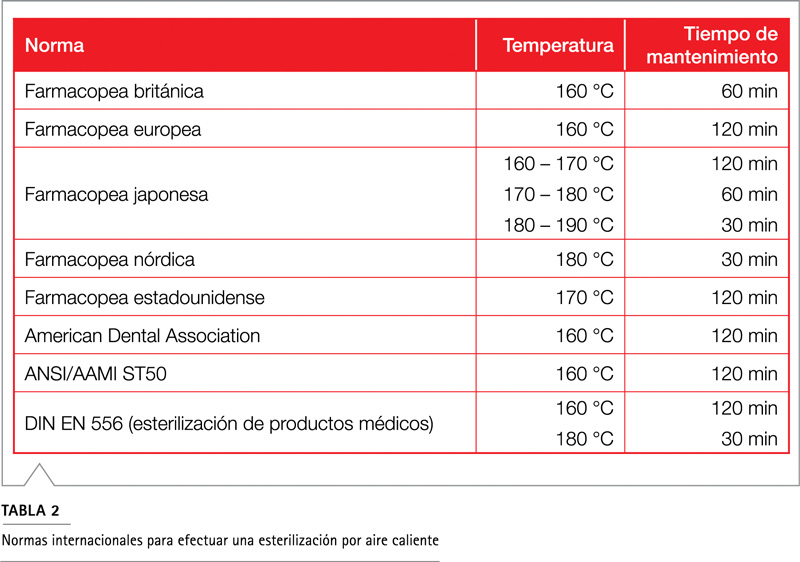
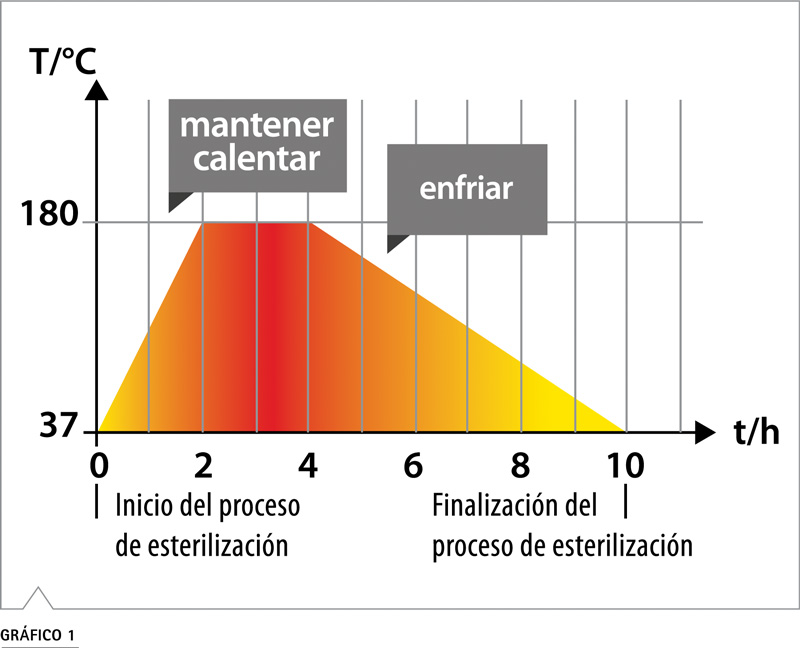
La esterilización por aire caliente a temperaturas entre 160 y 180 °C es el único de los procedimientos anteriormente mencionados que cumple las directivas sobre esterilización de equipos para aplicaciones médicas o farmacéuticas (tab. 2). El programa de esterilización de una incubadora consta de tres fases: calentamiento a la temperatura máxima que se puede alcanzar en cada parte del interior; tiempo de mantenimiento de la temperatura máxima para desactivar de manera efectiva el material biológico; y fase de enfriamiento a 37 ºC, tras la cual el equipo está preparado para la siguiente incubación. En los programas de esterilización por aire caliente de las incubadoras de CO2 se ha podido constatar la eliminación completa de los gérmenes de prueba anteriormente descritos5.
Diversas normas y farmacopeas recomiendan temperaturas de esterilización de 160 a 180 °C, con un tiempo de mantenimiento de hasta dos horas. Por consiguiente, con dos horas de acción de aire caliente a 180 ºC, se superan todas las normas que existen al respecto.
Medidas para evitar la contaminación mediante incubadoras de CO2
La aplicación de calor seco a 120 – 140 °C no constituye una esterilización conforme a las normas, pero sí consigue una considerable reducción de los gérmenes. En el caso de las esporas de Bacillus subtilis var. Niger, se apreció una reducción de hasta 106 veces con aire caliente a 140 °C6.
La desinfección con calor húmedo a 90 – 95 °C no es comparable, por su efectividad, a una esterilización por vapor en autoclave a 121 °C. A 90 °C se reduce notablemente el número de gérmenes, aunque no se desactivan por completo muchas esporas resistentes al calor como Bacillus subtilis y B. stearothermophilus5,10.
Peróxido de hidrógeno-(H2O2). Es habitual emplear vapor para descontaminar salas blancas7.
La desinfección por H2O2 adaptada a incubadoras de CO2 requiere, tras su aplicación, la desactivación segura y completa del vapor de H2O2, corrosivo y citotóxico, por ejemplo mediante radiación UV-C.
Medidas para evitar la contaminación mediante incubadoras de CO2
Desinfección UV mediante radiación UV-C a 253,7 nm: están comprobados los efectos mutagénicos de la radiación UV. Sin embargo, la eficacia depende de la radiación directa, ya que la profundidad de penetración es mínima y, por ello, solo es apta para el tratamiento de superficies. Se ha demostrado su efectividad en el tratamiento de agua en sistemas de humidificación de incubadoras de CO28. No obstante, Wallhäußer et. al. advierten de una mayor eficacia de la radiación UV con valores de humedad relativa del aire > 80 % 4.
El uso de filtros HEPA (High Efficiency Particulate Airfilter) con un determinado grado de separación es un procedimiento reconocido para reducir la concentración de partículas en salas blancas y cabinas de bioseguridad. En la incubadora de CO2 hay un ventilador que aspira el aire de la incubadora a través de un filtro HEPA y retiene las partículas de un tamaño determinado. Se ha demostrado una cierta eficacia de las incubadoras de CO29 como protección continua contra la contaminación.
A través de la oxidación, las superficies de cobre liberan iones de metales pesados bactericidas que impiden el desarrollo de bacterias en lugares húmedos. No obstante, los iones de cobre liberados también son tóxicos para las células cultivadas. Una serie de pruebas demostró la efectividad de las aleaciones de cobre/acero inoxidable sobre gérmenes de prueba seleccionados 8, pero la toxicidad depende directamente del contenido de cobre de la aleación12.
Límite de humedad: una incubadora de CO2 tiene que garantizar, por una parte, una humedad lo más alta posible para evitar la evaporación del medio. Por otra parte, no debe producirse una condensación incontrolada en su interior. Esto requiere un límite de humedad en un sistema de humedad pasivo sobre una superficie de agua abierta, como se da habitualmente en las incubadoras de CO2. Lo ideal es que el exceso de humedad pueda condensarse en un punto determinado que resulte fácil de controlar. Los microbios no pueden crecer en superficies secas.
Diseño sencillo: cuanto más complejas sean las estructuras y mayor sea la suma de todas las superficies del interior, mayor será el requerimiento de limpieza y el riesgo de contaminación. Por ello, minimizar la superficie interior y suprimir las estructuras es una medida muy eficaz para evitar la contaminación de manera continuada.
Seguridad de procesos, efectividad y costes de los diferentes conceptos de descontaminación
En el ámbito de las tareas de gestión de la contaminación, al usuario final le interesa especialmente la facilidad de uso, la seguridad del proceso, la efectividad y los bajos costes derivados. A continuación se analiza la idoneidad de las medidas y procedimientos anteriormente descritos (tab. 3). Se consideran cuatro conceptos diferentes típicos del mercado que representan la máxima dotación de un tipo de equipo.
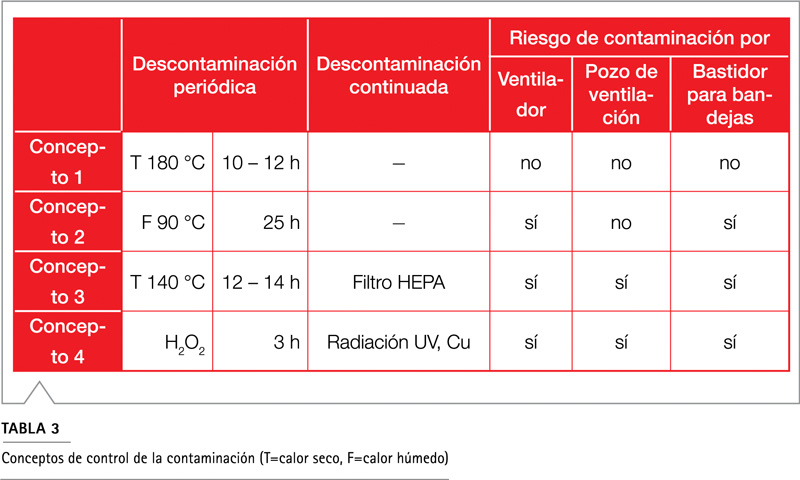
El concepto 1 ofrece únicamente una esterilización segura. Diez horas después de presionar el botón de inicio del programa de esterilizando, se consigue una incubadora limpia de microbios y lista para operar, sin ningún organismo extraño. En este concepto se prescinde conscientemente de otro equipamiento técnico para luchar contra la contaminación. En su lugar, se reduce notablemente el riesgo de contaminación minimizando las superficies y renunciando a estructuras. La supresión de un ventilador supone menor movimiento del aire en el interior, lo que disminuye el riesgo de transmisión de gérmenes por el aire y, de este modo, hace innecesario el uso de un filtro de partículas. En este sistema no hay ni muchos consumibles, piezas de desgaste, ni etapas de descontaminación complicadas ni de larga duración. Así de cómodo resulta trabajar con la incubadora con bajos costes operativos.
Con este concepto, es el cultivo de células lo que tiene prioridad para el usuario, no la incubadora de CO2. La seguridad es alta, los procesos de trabajo sencillos y los costes operativos bajos.
Seguridad de procesos, efectividad y costes de los diferentes conceptos de descontaminación
El calor húmedo en el concepto 2 requiere, en la práctica, un ciclo de más de 24 horas de duración, además de, por lo general, la calibración posterior del sistema sensor de CO2. El líquido de condensación que se origina en el interior al enfriarse el vapor de agua entraña riesgo de recontaminación de las superficies tratadas. Por eso, el fabricante recomienda desinfectarlo después mediante un proceso de pulverización/limpieza con un paño esterilizado. El ventilador y el bastidor para bandejas aumentan el riesgo de contaminación y las tareas de limpieza.
Este concepto no ofrece una gran seguridad, en su conjunto, y requiere a la vez los tiempos de inactividad más largos.
El concepto 3 se basa en un filtro de partículas que filtra continuamente los gérmenes del aire que entran, presentes en cierta medida por todas partes. Este filtro HEPA “recoge” únicamente gérmenes y esporas que deberán eliminarse finalmente a través de un cambio de filtro costoso en el equipo. De esta forma, los costes aumentan en función del grado de minuciosidad del usuario. Para aplicar la tecnología HEPA se necesitan ventiladores y pozos de aire que aumentan el riesgo de contaminación y el gasto de mantenimiento, ya que están llenos de recovecos y son difíciles de limpiar. Según necesidad, el interior puede descontaminarse con aire caliente a 140 °C durante 14 horas, pero no puede esterilizarse.
Con este concepto, la seguridad parece elevada porque se filtran los gérmenes que penetran por el aire. No obstante, esto conlleva la presencia de componentes que favorecen la formación de nidos de contaminación ocultos.
Seguridad de procesos, efectividad y costes de los diferentes conceptos de descontaminación
En el concepto 4 se combinan dos procedimientos reconocidos que tienen su origen en la tecnología de esterilización: descontaminación por vapor de peróxido de hidrógeno y radiación
La exposición a vapor de H2O2 es, con tres horas, el método de descontaminación más rápido, ya que no requiere tiempos de calentamiento y refrigeración. El uso de H2O2 ha de dejarse en manos de trabajadores cualificados, para evitar peligros al personal o en los cultivos de células. El equipo de radiación UV necesario para desactivar el peróxido de hidrógeno corrosivo y citotóxico lleva a cabo, además, la descontaminación periódica de la corriente de aire, pero conlleva que el interior de la incubadora sea más complejo y propenso a averías. Este sistema requiere un ventilador, lo que supone un mayor movimiento del aire y mayor riesgo de contaminación por gérmenes en el aire. Los bastidores para bandejas y los pozos de aire presentan recovecos que ocultan nidos de contaminación. Por último, los costes operativos de los reactivos de H2O2 y de las lámparas UV aumentan en función de lo cuidadosamente que se apliquen las medidas para evitar la contaminación.
Este concepto ofrece los tiempos de inactividad más cortos junto con un elevado esfuerzo técnico. La consiguiente elevada complejidad del sistema lo hace propenso a sufrir averías y sus costes operativos son los más elevados si se comparan los 4 conceptos.
El concepto de BINDER para minimizar el riesgo de contaminación
Las incubadoras de CO2 ofrecen un concepto concluyente (véase el concepto 1) que garantiza una desinfección periódica, sencilla y rápida, y permite una fácil autoesterilización. Renunciando, por lo tanto, a consumibles de elevado coste, como el filtro HEPA, las lámparas UV o el peróxido de oxígeno, se favorece un uso regular a largo plazo. El concepto BINDER convence por la combinación de los siguientes elementos:
- Fácil desinfección rutinaria: la cámara interna no presenta juntas, soldaduras, aristas, cantos, pozos de aire ni estructuras. Por eso se limpia rápidamente y sin esfuerzo con una desinfección de tipo pulverización/limpieza.
- Esterilización segura: la efectiva rutina de autoesterilización por aire caliente a 180 ºC cumple las directivas internacionales para productos médicos. El equipo cuenta incluso con el moderno sensor de CO2 con tecnología IR precisa que también se esteriliza (nueva serie CB).
- Minimización radical de la superficie: al prescindir de estructuras como bastidores para bandejas, conductos de aire, ventiladores, filtros HEPA y lámparas UV, se reducen al mínimo las superficies del interior de la incubadora a las que podrían adherirse microbios o esporas.
- Ausencia absoluta de condensación: el sistema patentado de humidificación de doble cubeta genera una elevada humedad y limita al mismo tiempo el punto frío al 95 %. De este modo, las paredes interiores permanecen secas, incluso en las esquinas.
Conclusiones finales
En publicaciones recientes11 se ha hecho especial hincapié en el aspecto de la duración total de la rutina de descontaminación y en la necesidad de una descontaminación continuada. Sin embargo, desde una perspectiva crítica, no deben ignorarse tampoco la duración real del proceso ni los costes derivados del reequipamiento de los componentes del proceso de descontaminación que requieren mucho mantenimiento, así como el tiempo de trabajo y la vulnerabilidad del sistema.
En este texto se han comparado diferentes conceptos anticontaminación para incubadoras de CO2 desde el punto de vista del usuario. Es imposible evitar la contaminación al 100 %, pero se le facilita considerablemente al usuario el buen cuidado del cultivo de células. El equipo debe ser fácil de usar, robusto y fiable, y ofrecer seguridad a largo plazo. El coste necesario para conseguir esto depende en gran medida del concepto concluyente para evitar la contaminación.
Autor
Jens Thielmann es licenciado en Biología y jefe de producto del área de Crecimiento y Almacenamiento de BINDER GmbH. Es responsable de producto para las diferentes incubadoras que se emplean en la investigación médica, científica y farmacéutica para la incubación de bacterias o cultivos celulares de mamíferos, así como de los congeladores a temperaturas ultrabajas para el almacenamiento estable de muestras sensibles a largo plazo.
Referencias a directivas internacionales
British Pharmacopoeia Commission Methods of Sterilization. Londres (Reino Unido): Ap. X VIII, 2003
Pharmcopeia Europea 7a edición, 2010
Japanese Pharmacopoeia www.jpdb.nihs.go.jp/jp14e
Pharmacopoeia Nordica Online Reference en www.dekker.com
US Pharmacopoeia www.usp.com
American Dental Association www.ada.org
Association for the Advancement of Medical Instrumentation (AAMI) www.aami.org
Deutsches Institut für Normung e.V. (DIN) www.din.de
Fuentes
1 Leitfaden für die Gute Herstellungspraxis, EU-GMP Leitfaden ISBN-10: 3-934971-24-5 Maas & Peither GMP-Verlag
2 S. Coecke et. al., Guidance on Good Cell Culture Practice, A Report of the Second ECVAM Task Force on Good Cell Culture (GCCP), ATLA 33, 261-287, 2005
3 Directiva de la Comisión Europa sobre donación de células y tejidos: 29/03/2005: en relación con la fijación de estándares de calidad para donación, obtención, evaluación, procesamiento, conservación, almacenamiento y distribución de células y tejidos humanos.
4 K.H. Wallhäußer Praxis der Sterilisation, Desinfektion – Konservierung, Keimidentifizierung – Betriebshygiene, 5ª edición 1995
5 P. Distler, 180 °C Hot air sterilization: a safe method against microbiological contamination in CO2 incubators Lab Asia, noviembre de 2003, p. 11
6 J. Dalamasso, APEX Laboratories, Effective Heat Sterilization in CO2 Incubators, Vol. 4, Nr. 3, Thermo Electron Corporation’s Heat Sterilization White Paper, 2003
7 D.M.Carlberg, Cleanroom Microbiology for Non-Microbiologists, CRC Press, 2005
8 H. Basujima, D. Mistry, Technical Development Report, Sanyo Electric Biomedical Co., Ltd. A Comparative Analysis of Ultraviolet Light Decontamination versus High-Heat Sterilization in the Cell Culture CO2 Incubator, with the Use of Copper-Enriched Steel Construction to Achieve Background Contamination Control™, 2007
9 A. Campbell, D. Figel, Importance of Class 100 Air in a CO2 Incubator, Vol. 4, Nr. 1, Thermo Electron Corporation’s Class 100 Air White Paper, 2003
10 Bio safety Investigation Unit, CAMR, Efficacy of a CO2 incubator heat disinfection cycle on dried microbes, 1998
11 Schaffung eines sicheren Umfelds für Zellkulturen in biopharmazeutischen Anwendungen, White Paper Panasonic, Laborpraxis September 2013
12 H.T. Michels, Anti-Microbial Characteristics of Copper; ASTM Standardization News, Oktober 2006; www.tellurex.com
Acerca de las Incubadoras de CO2. Serie C | CB de BINDER
Incubadoras CO2 CB 170
CARACTERÍSTICAS IMPORTANTES
- Rango de regulación de la temperatura: 4 °C por encima de la temperatura ambiente hasta 60 °C
- Rango de regulación de CO2: 0-20 % vol. CO2
- Rango de regulación de O2: 0,2-20 % vol. O2 (Variante)
- Concepto anticontaminación probado con esterilización por aire caliente a 180 °C
- Controlador de pantalla táctil de manejo intuitivo
- Gestión optimizada de la humedad con tiempo de recuperación
- Capacidad interior ampliada a 170 litros ocupando el mismo espacio
- Altura de apilado de solo 1,80 m para un buen manejo del equipo superior
- Sistema de autodiagnóstico Fail Safe CO2 para proteger los cultivos celulares
- Sistema DuoDoor™: puerta exterior y puerta de cristal con apertura en un solo movimiento
VENTAJAS A SIMPLE VISTA
Controlador intuitivo con pantalla táctil
La más moderna tecnología de regulación con programación a intervalos y en tiempo real. Registro interno de datos, valores de medición en formato abierto, seleccionables a través de USB.
Cierre de puerta DuoDoor™
Con el nuevo cierre ergonómico de la puerta, la puerta exterior y la puerta interior de cristal se pueden abrir simultáneamente.
Gestión de la humedad con tiempo de recuperación rápido
Sistema humectante Permadry™ perfeccionado, con práctico recipiente de agua que asegura una humidificación acelerada tras la apertura de la puerta.
Trabajar cómodamente en el laboratorio
La altura reducida del equipo permite trabajar cómodamente con el equipo superior apilado.
Todas las incubadoras de CO2 de BINDER garantizan unas condiciones de crecimiento óptimas y reproducibles para el cultivo de células. El nuevo sistema de calentamiento de envoltura de silicona se encarga, junto con la tecnología Permadry, de que no haya condensación. Gracias a la esterilización por aire caliente a 180 °C, se eliminan con fiabilidad las bacterias y esporas cuando es necesario.
La extraordinaria cámara interna de una pieza, sin estructuras incómodas, hace que la limpieza sea muy sencilla. Las incubadoras de CO2de las series C y CB ofrecen grandes ventajas para el cultivo celular y de tejidos con una calidad constante.
VENTAJAS A SIMPLE VISTA
MÍNIMO RIESGO DE CONTAMINACIÓN
Serie C, CB
Con la esterilización por aire caliente a 180 °C, se esteriliza todo el interior con solo pulsar un botón. En la serie CB también se esteriliza el sensor de CO2.
ÓPTIMO CULTIVO CELULAR
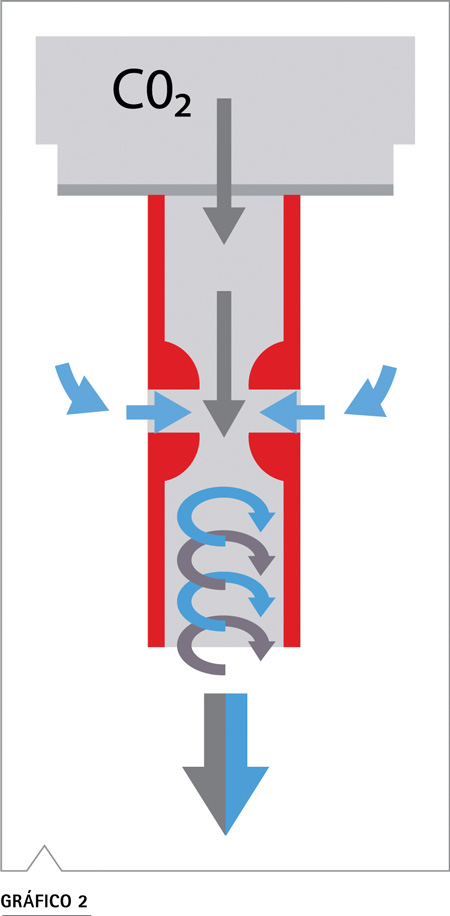
Serie C, CB
Gracias a un valor de PH constante y a una tecnología de medicion estable del CO2, así como la distribución homogénea del CO2 mediante un cabezal de mezcla de gas BINDER que funciona según el principio Venturi.
GESTIÓN DE HUMEDAD PATENTADA

Serie CB
Gracias a unos valores de humedad elevados del 90 al 95 % h.r., el medio se evapora mínimamente.
El límite de humedad activo mediante el sistema de humedad Permadry™ con doble capa hace que las paredes internas se mantengan secas.
CONCEPTO DE CÁMARA INTERIOR “MENOS ES MÁS”

Serie CB
Garantiza una limpieza rápida y sencilla gracias a una cámara interna de una sola pieza, sin soldaduras, de acero inoxidable y sin estructuras molestas. No se necesitan consumibles.
Serie C | Incubadoras de CO2 con esterilización por aire caliente
Las incubadoras de la serie C son idóneas para las aplicaciones rutinarias de cultivo de células: están libres de contaminación gracias a la esterilización por aire caliente a 180 °C y con un nivel de estabilidad del pH fiable gracias al sistema de medición por infrarrojos y CO2 sin deriva.
Modelo C 170
CARACTERÍSTICAS IMPORTANTES
- Rango de temperatura: desde 7 °C por encima de la temperatura ambiente hasta 50 °C• Rango de humedad: hasta 95 % h.r.
- Autoesterilización por aire caliente a 180 °C
- Sistema de Humidificación sin condensación
- Tubo de mezcla de gas de CO2 con efecto Venturi
- Sensor de CO2 con tecnología de infrarrojos
- Indicador LED de 3 dígitos con 7 segmentos
- Puerta con tope a izquierda o derecha
- Puerta interior estanca de vidrio de seguridad (ESG)
- Cámara interna de una pieza sin soldaduras de acero inoxidable
Serie CB | con esterilización por aire caliente y sensor de CO2 con esterilización térmica
La serie CB de BINDER es idónea para todas las aplicaciones de incubación delicadas y garantiza el mejor crecimiento celular. Además, gracias a su amplio abanico de opciones y accesorios, las incubadoras de BINDER también permiten realizar cultivos complejos o ambientes de crecimiento individuales bajo condiciones hipóxidas.
CARACTERÍSTICAS IMPORTANTES
- Rango de temperatura: desde 4 °C por encima de la temperatura ambiente hasta 60 °C (CB 170)
- Rango de humedad: de 90 hasta 95 % h.r.
- Rango de regulación de CO2: 0-20 % vol. CO2
- Rangos de regulación de O2 alternativos: 0,2-20 % vol. O2 o 10- 95 % vol. O2 (variantes de O2)
- Concepto anticontaminación probado con esterilización por aire caliente a 180 °C
- Sistema de humidificación optimizado de doble bandeja con protección antirrocío
- Tobera de mezcla de gas de CO2 con efecto Venturi
- Sensor de CO2 esterilizable por aire caliente con tecnología de Infrarrojos
- Controlador de pantalla táctil de manejo intuitivo (CB 170)
EXTRACTO DE OPCIONES Y ACCESORIOS
Puerta interior con varias divisiones
Las puertas de vidrio divididas y sus correspondientes bandejas especiales permiten la división espacial de distintos experimentos. La atmósfera interior permanece estable. Serie CB
Adaptador de apilado
Los adaptadores de apilado contribuyen a ahorrar espacio en la instalación y al apilado seguro de las incubadoras de CO2de BINDER. Serie C, CB
Cambiador de botellas de gas
BINDER Gas Supply Service para la conexión de dos botellas de gas a un máximo de dos incubadoras, con alarma óptica y acústica, así como con salida de alarma sin voltaje. Serie C, CB
Agitador de CO2
Solución de alta calidad para la incubación de cultivos celulares en suspensión en incubadoras de CO2. Gracias al uso exclusivo de componentes resistentes a la corrosión en cajas de acero inoxidable, el agitador de CO2 es especialmente apto para incubadoras de gasificación con elevadas concentraciones de CO2 y una humedad del aire prácticamente saturada. Serie C, CB
Adaptadores interiores de cobre
El conjunto se compone de tres bandejas de cobre y un recipiente de agua revestido de cobre. Con el equipamiento de cobre, se reduce el esfuerzo de limpieza de la incubadora sin detrimento de la elevada seguridad contra la contaminación. Serie C
Servicios
Puede solicitar los servicios de instalación, mantenimiento, calibración, validación o de garantía en el marco de un contrato de servicio de mantenimiento o por separado. Encontrará más información en el capítulo Accesorios y servicios. Serie C, CB.

Autor:
Jens Thielmann
Más información:
info@wasserberg.com
www.wasserberg.com
Solicite cotización sin cargo por Incubadora de CO2 haciendo click aquí
Artículos relacionados:
Analizadores de trazas para H2O, H2, O2, CH4, CO2, CO, C2H2
La nueva generación de incubadoras Hettcube de Hettich
Analizadores de carbono / hidrógeno / azufre Eltra. El especialista en análisis elemental