En el lado seguro: Cumpliendo con los requisitos de FDA – CFR 21 parte 11 utilizando las soluciones de testo Saveris para pharma

CFR 21 Parte 11: Cumplimiento de todos los requisitos.
La fabricación de productos farmacéuticos se realiza en las más altas condiciones de calidad y seguridad. Instancias regulatorias como la Administración de Alimentos y Drogas (FDA) en los EE. UU. definen cómo se deben implementar estos requisitos. La documentación ininterrumpida y a prueba de falsificación de todo el proceso de valor agregado juega un papel clave en esto.
Desde el punto de vista de la documentación electrónica de la Administración de Medicamentos y Alimentos (FDA) de EE. UU. debe estar regulado de una manera particular. En 1997, con el fin de garantizar la confiabilidad de los registros almacenados y firmados electrónicamente, la FDA creó un catálogo vinculante de requisitos: Registros electrónicos y firma 21 CFR Parte 11[1]. Este reglamento no solo establece el marco técnico en el que la documentación electrónica puede ser creado, firmado y archivado con el más alto nivel de prueba requerido contra la falsificación y los controles de acceso seguro. También exige controles administrativos y de procesos adicionales, como los procedimientos operativos estándar (SOP) y la capacitación de los usuarios. Solo cuando los sistemas técnicos adecuados se combinan con los SOP adaptados al proceso respectivo, el cumplimiento está completo de los requisitos de la FDA para los fabricantes de productos farmacéuticos garantizados.
Este documento técnico describe principalmente los requisitos técnicos de los Registros electrónicos y la Regla de firma 21 CFR Parte 11 y cómo se implementan en el monitoreo ambiental con testo Saveris Pharma Solutions.
Muchos de nuestros clientes que están sujetos a las regulaciones de la FDA confían en las soluciones Saveris Pharma de testo para sus tareas de monitoreo ambiental. Con el software testo Saveris CFR, el sistema de monitoreo de datos de medición automatizado y completamente libre de papel ofrece funciones integradas que cumplen con los requisitos de la FDA y, por lo tanto, tiene capacidad de validación. Esto facilita considerablemente que nuestros clientes cumplan los requisitos respectivos de forma sostenible y sin interrupciones; sino también para pasar de la documentación en papel a la electrónica.
Alcance y criterios de la normativa CFR.
11.1 Alcance
(a) Las regulaciones en esta parte establecen los criterios bajo los cuales la agencia considera registros electrónicos, firmas electrónicas, y firmas manuscritas ejecutadas en registros electrónicos para que sean confiables, confiables y generalmente equivalentes a registros en papel y firmas manuscritas ejecutadas en papel.
(b) Esta parte se aplica a los registros en formato electrónico que se crean, modifican, mantienen, archivan, recuperan o transmiten, según los requisitos de registros establecidos en los reglamentos de la agencia. Esta parte también se aplica a los registros electrónicos presentados a la agencia según los requisitos de la Ley Federal de Alimentos, Medicamentos y Cosméticos y la Ley de Servicios de Salud Pública, incluso si dichos registros no están específicamente identificados en los reglamentos de la agencia. Sin embargo, esta parte no se aplica a los registros en papel que se transmiten o se han transmitido por medios electrónicos.
(c) Cuando las firmas electrónicas y sus registros electrónicos asociados cumplan con los requisitos de esta parte, la agencia considerará que las firmas electrónicas son equivalentes a las firmas manuscritas completas, iniciales y otras firmas generales según lo exijan los reglamentos de la agencia, a menos que exista una excepción específica en el (los) reglamento (s) vigente a partir del 20 de agosto de 1997.
(d) Los registros electrónicos que cumplan con los requisitos de esta parte se pueden utilizar en lugar de registros en papel, de acuerdo con 11.2, a menos que los registros en papel sean específicamente requeridos.
(e) Los sistemas informáticos (incluidos el hardware y el software), los controles y la documentación del asistente que se mantienen bajo esta parte deben estar disponibles para la inspección de la FDA y estar sujetos a esta.
testo Saveris – diseñado para cumplir plenamente con 21 CFR Parte 11
El software testo Saveris ha sido diseñado para cumplir con los requisitos de 21 CFR Parte 11 con respecto a los registros electrónicos y las firmas electrónicas durante su vida útil. Para lograr y mantener el cumplimiento total de CFR, los requisitos organizativos y técnicos deben cumplirse:
- Cumplir con los requisitos de la organización significa que las compañías farmacéuticas establecerán estructuras organizativas y definirán, describirán y documentarán todos los procesos para demostrar qué medidas de protección utiliza la empresa respectiva para cumplir con las regulaciones y cómo se aplican. El núcleo de dicha documentación consiste en Procedimientos Operativos Estándar (SOP), que describen y regulan todos los procesos en detalle. Estos describen en detalle cómo las personas responsables deben llevar a cabo y utilizar los procesos y sistemas para cumplir con los requisitos que se les imponen.
- El cumplimiento de los requisitos técnicos significa que el cumplimiento de los requisitos en el nivel técnico se basa en el uso de productos que ya son adecuados para esta área según el fabricante, por ejemplo. Testo Saveris Pharma Solutions.
- Los beneficios del sistema de monitoreo de datos testo Saveris incluyen documentación centralizada segura y una gama de diferentes opciones de alarma. El sistema garantiza la detección, el almacenamiento y el archivo fiables de los datos de medición en los procesos de producción, al almacenar y transportar productos farmacéuticos. Por lo tanto, las soluciones de Testo Saveris cumplen con los requisitos de 21 CFR Parte 11 y permiten a los usuarios ahorrar tiempo y dinero con una gestión de datos de medición automatizada totalmente compatible.
Preparado para una posible auditoría de la FDA: Certificado de validación de software.
Sistema de monitoreo de datos de medición probado con certificado: el Instituto Fraunhofer de Ingeniería de Software Experimental confirma que el sistema de monitoreo de datos de medición de Testo Saveris cumple con los requisitos de 21 CFR Parte 11. Las pruebas se llevaron a cabo de acuerdo con las pautas de evaluación del grupo de interés especial GAMP: Cumplimiento de 21 CFR Parte 11, Registros electrónicos y firmas electrónicas.

Documentos para apoyar su validación.
Estos documentos lo apoyan en la validación del sistema testo Saveris basado en GAMP5:
- Plantillas personalizables para análisis de riesgo.
- Plantillas de uso individual para:
- Plan maestro de validación
- Especificaciones de validación.
Cómo proceder con la presentación electrónica.
11.2 Implementación
(a) Para los registros que deben mantenerse pero no enviarse a la agencia, las personas pueden usar registros electrónicos en lugar de registros en papel o firmas electrónicas en lugar de firmas tradicionales, en todo o en parte, siempre que se cumplan los requisitos de esta parte.
(b) Para los registros presentados a la agencia, las personas pueden usar registros electrónicos en lugar de registros en papel o firmas electrónicas en lugar de firmas tradicionales, en su totalidad o en parte, siempre que:
(1) Se cumplen los requisitos de esta parte; y
(2) El documento o partes de un documento a ser enviado han sido identificados en el expediente público No. 92S-0251 como el tipo de presentación que la agencia acepta en formato electrónico. Este expediente identificará específicamente qué tipos de documentos o partes de documentos son aceptables para su presentación en formato electrónico sin registros en papel y la (s) unidad (es) receptora (s) de la agencia (por ejemplo, centro específico, oficina, división, sucursal) a la que se pueden enviar las presentaciones. Los documentos que envíen a la (s) unidad (es) de la agencia no especificados en el expediente público no se considerarán oficiales si se presentan en formato electrónico; Los formularios en papel de dichos documentos se considerarán oficiales y deberán acompañar cualquier registro electrónico.
Se espera que las personas consulten con la unidad receptora de la agencia prevista para obtener detalles sobre cómo (por ejemplo, el método de transmisión, los medios, los formatos de archivo y los protocolos técnicos) y si deben proceder con la presentación electrónica.
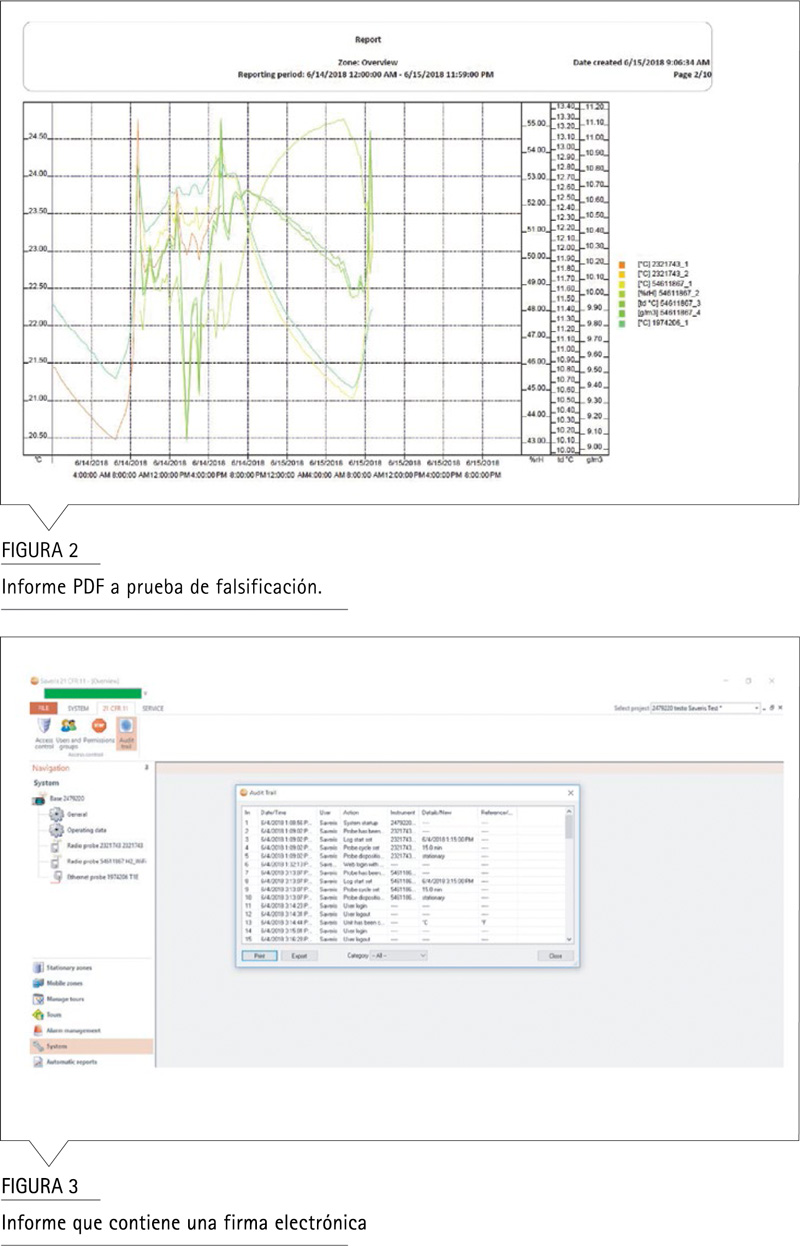
A prueba de falsificaciones y protegido de acceso: formato PDF.
El software testo Saveris CFR mantiene los datos (metadatos y datos sin procesar) en una base de datos segura y protegida por contraseña administrada por el departamento de TI del cliente. Puede, sin violar las pautas de la FDA, exportar copias de los documentos electrónicos como un Formato de Documento Portátil (PDF), y definir a la persona (s) con derechos de acceso a través de la firma electrónica correspondiente. Esto significa que no solo la integridad de sus datos, sino también el acceso a los contenidos, están protegidos de manera confiable.
testo Saveris ofrece las siguientes funciones de PDF:
- Reportes PDF automáticos (diario/semanal/mensual)
- Creación manual de informes en PDF para el tiempo definido por el usuario, protegido con contraseña maestra
- Impresiones compatibles con 21 CFR Parte 11
- Código de identificación para una clara asignación de informes en PDF.
Controles de usuario y acceso en el sistema cerrado
11.3 Definiciones
(a) Las definiciones e interpretaciones de los términos contenidos en la sección 201 de la ley se aplican a esos términos cuando se usan en esta parte.
(b) Las siguientes definiciones de términos también se aplican a esta parte:
(1) Ley significa la Ley Federal de Alimentos, Medicamentos y Cosméticos (secciones 201-903 (21 U.S.C. 321-393)).
(2) Agencia significa la Administración de Drogas y Alimentos.
(3) La biometría es un método para verificar la identidad de una persona basada en la medición de la (s) característica (s) física (s) o la (s) acción (es) repetible (s) en la que esas características y / o acciones son exclusivas de esa persona y son medibles.
(4) Sistema cerrado significa un entorno en el que el acceso al sistema está controlado por personas que son responsables del contenido de los registros electrónicos que se encuentran en el sistema.
(5) Firma digital significa una firma electrónica basada en métodos criptográficos de autenticación del originador, calculada mediante el uso de un conjunto de reglas y un conjunto de parámetros que permiten verificar la identidad del firmante y la integridad de los datos.
(6) Registro electrónico significa cualquier combinación de texto, gráficos, datos, audio, representación pictórica u otra representación de información en forma digital que se crea, modifica, mantiene, archiva, recupera o distribuye mediante un sistema informático.
(7) Firma electrónica significa una compilación de datos de computadora de cualquier símbolo o serie de símbolos ejecutados, adoptados o autorizados por un individuo como el equivalente legalmente vinculante de la firma manuscrita del individuo.
(8) Firma manuscrita significa el nombre o marca legal de un individuo escrito a mano por esa persona y ejecutado o adoptado con la intención actual de autenticar una escritura en forma permanente. Se conserva el acto de firmar con un instrumento de escritura o marcado, como un bolígrafo o un lápiz. El nombre o marca legal con guión, mientras se aplica convencionalmente al papel, también se puede aplicar a otros dispositivos que capturan el nombre o la marca.
(9) Sistema abierto significa un entorno en el que el acceso al sistema no está controlado por personas que son responsables del contenido de los registros electrónicos que se encuentran en el sistema.
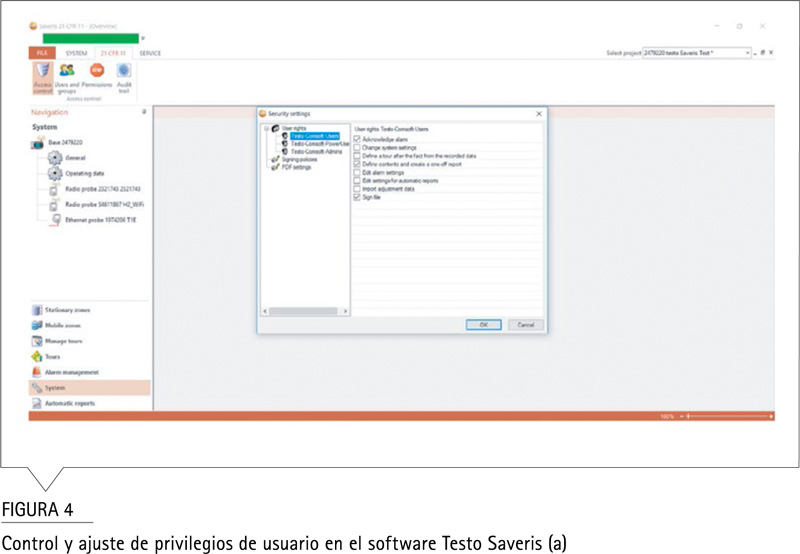
Acceso grupal controlado a través del sistema de seguridad de Windows.
La documentación de datos confidenciales con el software testo Saveris CFR generalmente se realiza en un entorno cerrado y controlado, denominado sistema cerrado. Dichos registros de datos pueden manejarse de manera segura en un entorno al que solo tiene acceso un grupo controlado de personas. Con el software testo Saveris CFR, el control de usuario / acceso se realiza a través del sistema de seguridad de Windows probado y probado que permite la asignación de ID de usuario, administración de derechos, administración de usuario y contraseña o autenticación de usuario. El administrador de TI determina el concepto de autorización (derechos de usuario, liberación o bloqueo de las funciones del software) para tres niveles de usuario en el software testo Saveris CFR.
Acceso individual a través de la autenticación LDAP.
Con respecto al acceso individual, el software testo Saveris CFR se basa en la política de inicio de sesión / cuenta e Windows, la política de seguridad, los requisitos de contraseña, la política de bloqueo de cuenta, etc.
El sistema utilizado debe validarse dentro de su entorno para garantizar precisión, confiabilidad y rendimiento. Los registros de datos no válidos o alterados deben identificarse a tiempo, ya sea de forma automática o mediante técnicas de validación adecuadas, y aislarse. Los servicios de solución al cliente de Testo ofrecen validación de software in situ junto con la documentación de calificación para la instalación de una solución de testo Saveris Pharma.
Incluido en el software testo Saveris están las siguientes características:
- Integración completa del concepto de acceso en el sistema de seguridad de Windows probado y probado (por ejemplo, administración de usuario y contraseña)
- Concepto de autorización: asignación de derechos por administrador para tres niveles de usuario
- Protocolo propio de Testo (propietario) con comunicación inalámbrica y ethernet.
- Almacenamiento de datos compatible con CFR con base de datos verificada por suma de comprobación
- Uso de sumas de comprobación para garantizar la transmisión correcta y segura de los datos.
- Copia de seguridad diaria automática y copia de seguridad manual de archivos de base de datos posible.
Cómo conectar testo Saveris CFR con el sistema de seguridad NT
- Los grupos locales se crean para conectar el software testo Saveris CFR con el sistema de seguridad NT: En la administración del sistema, se agregan tres grupos locales a los que ya existen: Testo-Comsoft-Admins, Testo-Comsoft-Power Usuarios y Testo-Comsoft-Usuarios.
- El software testo Saveris está registrado como una fuente de entradas de registro de eventos (registro de auditoría y registros de eventos).
- Un administrador o miembro del grupo local Testo-ComSoft-Admins puede activar o desactivar funciones individuales o posibilidades del sistema para grupos de usuarios configurados previamente en el nivel del sistema operativo.
Procesos y controles a prueba de falsificación en el sistema cerrado.
11.10 Controles para sistemas cerrados.
Las personas que usan sistemas cerrados para crear, modificar, mantener o transmitir registros electrónicos deben emplear procedimientos y controles diseñados para garantizar la autenticidad, integridad y, cuando sea apropiado, la confidencialidad de los registros electrónicos y para garantizar que el firmante no pueda rechazar fácilmente Registro firmado como no genuino. Tales procedimientos y controles deberán incluir lo siguiente:
(a) Validación de los sistemas para garantizar la precisión, la confiabilidad, el rendimiento esperado consistente y la capacidad de discernir registros inválidos o alterados.
Los servicios de solución al cliente de Testo brindan una amplia gama de servicios de validación en su país respectivo, como la calificación de instalación del sistema (IQ) y la calificación operacional (OQ). También apoyamos la validación de la computadora.
(b) La capacidad de generar copias precisas y completas de los registros en forma legible por humanos y en formato electrónico adecuado para la inspección, revisión y copia por parte de la agencia. Las personas deben comunicarse con la agencia si tiene alguna pregunta con respecto a la capacidad de la agencia para realizar dicha revisión y copia de los registros electrónicos.
Con testo Saveris, los informes de las áreas de temperatura se pueden exportar para que se lean como informes en PDF, mientras que sus datos sin procesar todavía se mantienen de forma segura en la base de datos. Las soluciones de transporte que contienen testo 184 como registrador de datos de viaje acceden a los datos del viaje en un informe PDF y cargan los datos en la base de datos central y segura para futuras auditorías.
(c) Protección de registros para permitir su recuperación precisa y lista durante todo el período de retención de registros.
La base de datos es administrada por el departamento de TI del cliente y debe seguir las pautas relacionadas con el período de retención de registros. El sistema admite tanto las reglas de copia de seguridad automática como la copia de seguridad manual.
(d) Limitar el acceso del sistema a personas autorizadas.
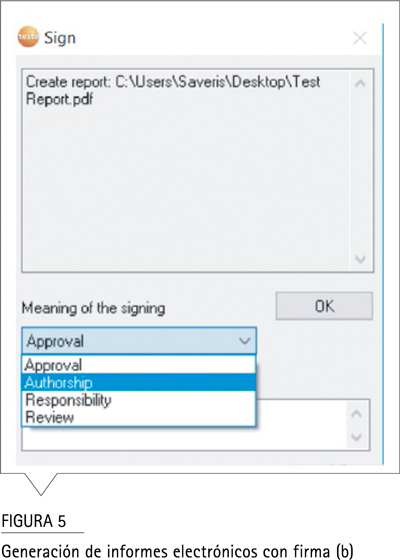
(e) Use of secure, computer-generated, time-stamped audit trails to independently record the date and time of operator entries and actions that create, modify, or delete electronic records. Record changes shall not obscure previously recorded information. Such audit trail documentation shall be retained for a period at least as long as that required for the subject electronic records and shall be available for agency review and copying.
El software testo Saveris rastrea automáticamente todas las actividades del usuario en el sistema. Una pista de auditoría documenta los componentes de testo Saveris, la hora y el nombre de usuario de cada evento y la actividad realizada.
(f) Uso de verificaciones del sistema operacional para hacer cumplir la secuencia permitida de pasos y eventos, según corresponda.
(g) El uso de los controles de autoridad para garantizar que solo las personas autorizadas puedan usar el sistema, firmar electrónicamente un registro, acceder a la operación o al dispositivo de entrada o salida del sistema informático, alterar un registro o realizar la operación en cuestión.
(h) El uso del dispositivo (por ejemplo, el terminal) verifica para determinar, según corresponda, la validez de la fuente de entrada de datos o la instrucción operativa.
(i) Determinación de que las personas que desarrollan, mantienen o usan sistemas de registro electrónico / firma electrónica tienen la educación, la capacitación y la experiencia para realizar las tareas asignadas.
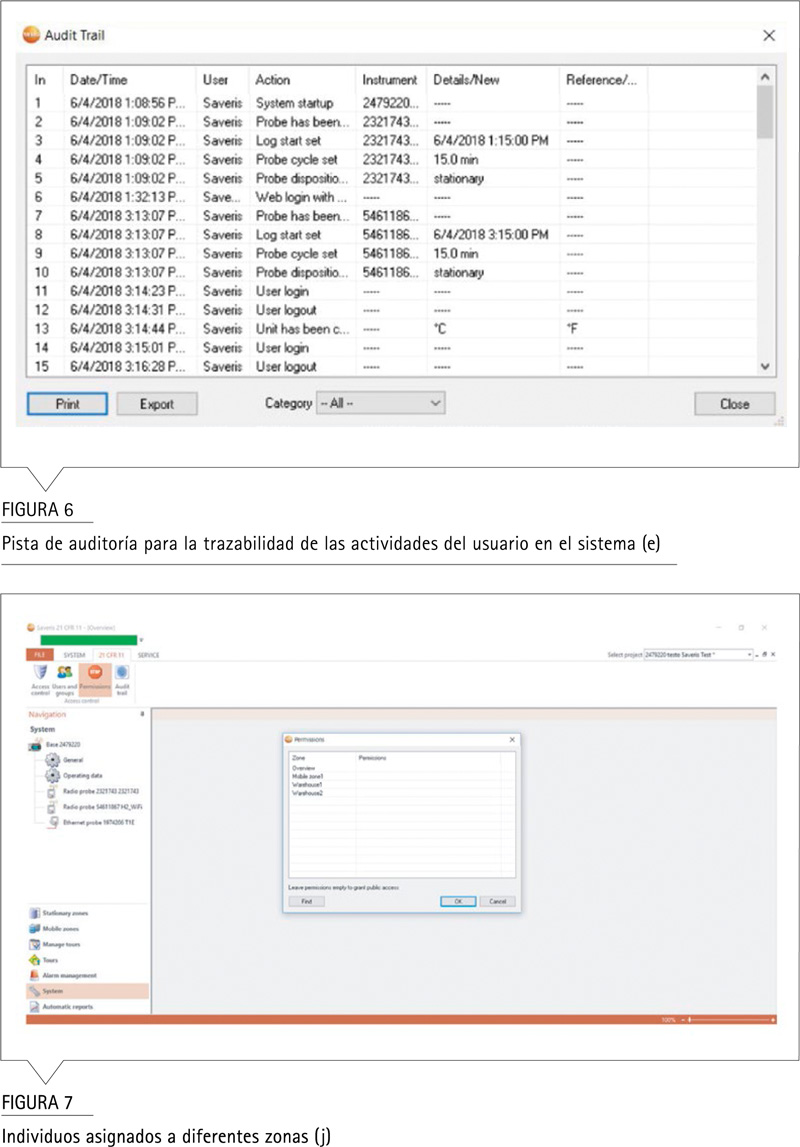
(j) El establecimiento y la adherencia a políticas escritas que responsabilizan a las personas y son responsables de las acciones iniciadas bajo sus firmas electrónicas, a fin de impedir la falsificación de registros y firmas.
Además de los controles y componentes técnicos de testo, las soluciones de Saveris Pharma le ofrecen la conformidad con las regulaciones de CFR, por lo que el usuario siempre necesita controles adicionales. Estos incluyen políticas escritas y procedimientos operativos estándar para asegurarse de que las personas puedan ser responsables de las firmas que iniciaron.
(k) Uso de controles apropiados sobre la documentación de los sistemas, incluyendo:
(1) Controles adecuados sobre la distribución, el acceso y el uso de la documentación para el funcionamiento y mantenimiento del sistema.
(2) Revisar y cambiar los procedimientos de control para mantener una pista de auditoría que documente el desarrollo y la modificación de la secuencia de tiempo de la documentación de los sistemas.
Aplicación segura en sistemas abiertos
11.30 Controles para sistemas abiertos
Las personas que utilizan sistemas abiertos para crear, modificar, mantener o transmitir registros electrónicos deben emplear procedimientos y controles diseñados para garantizar la autenticidad, integridad y, según corresponda, la confidencialidad de los registros electrónicos desde el momento de su creación hasta el punto de su creación. recibo.
Dichos procedimientos y controles incluirán aquellos identificados en 11.10, según corresponda, y medidas adicionales, como el cifrado de documentos y el uso de estándares de firma digital adecuados para garantizar, según sea necesario en las circunstancias, la autenticidad, integridad y confidencialidad de los registros.
testo Saveris: un sistema cerrado incluso en entornos abiertos.
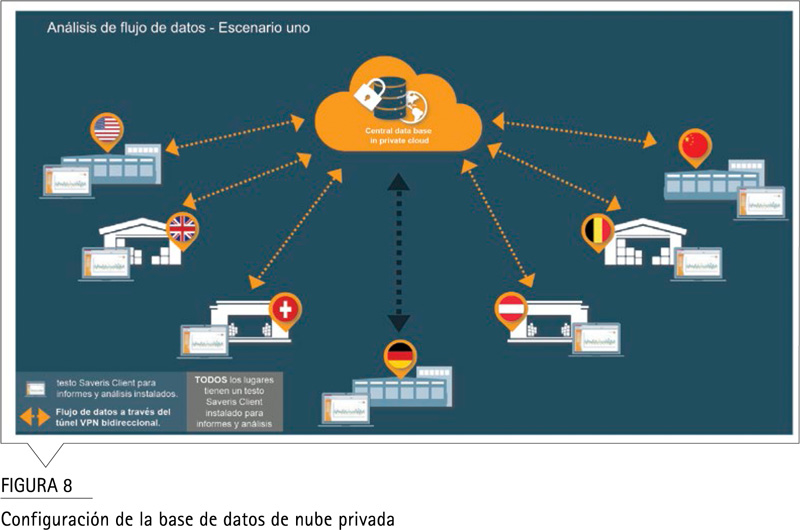
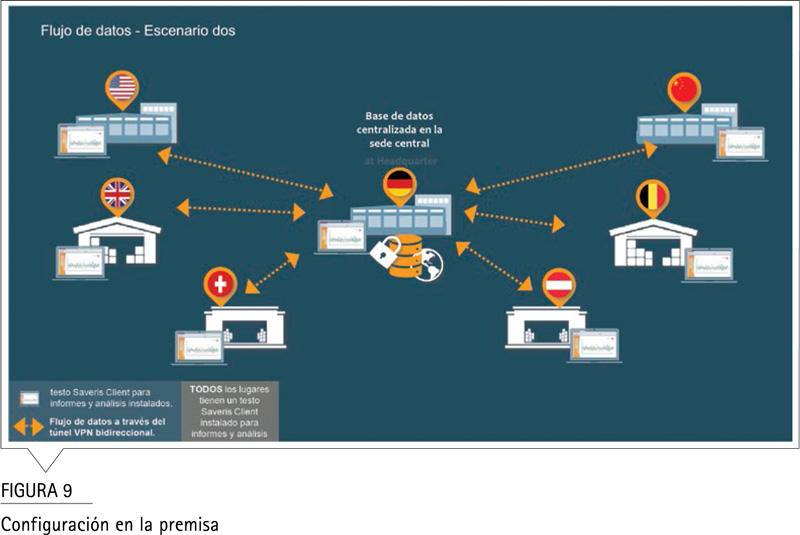
Las soluciones de testo Saveris Pharma alojan los datos de forma centralizada en un sistema cerrado que admite dos posibilidades diferentes: en las instalaciones administradas por la TI del cliente y la nube privada.
Si la opción es para una nube privada, significa que los datos se almacenan en un servidor administrado por un tercero. Si la opción es para este tipo de alojamiento, se realizará una evaluación para garantizar que las políticas de seguridad del proveedor se ajusten a las pautas de GxP y a los requisitos de la norma FDA 21 CFR Parte 11.[2] Nuestros ingenieros pueden aconsejarle sobre cómo configurarlo mejor. De esta manera, ambos se consideran un sistema cerrado, ya que están bajo la administración del cliente y son accesibles solo por usuarios autorizados en su dominio de AD.
Para los clientes que envían productos a destinos que no están en la misma infraestructura de TI y cuando no se pudo establecer una conexión VPN, nuestra solución de Testo Saveris Pharma Transport también se puede configurar para usar la función Bucket.
A diferencia del alojamiento de datos, esta funcionalidad usa depósitos solo como una forma de transferir datos desde múltiples ubicaciones a la base de datos central. Un Cubo se llena temporalmente con datos y, tan pronto como estos datos se sincronizan con la Base de Datos Central, se eliminan del cubo. Testo garantiza la seguridad de extremo a extremo de los datos de los registradores de transporte.
En este escenario, se puede usar un grupo como el que proporciona Amazon Web Services para configurar los registradores en origen y leerlos en múltiples destinos.[3]
Firmando y enlazando firmas de registros electrónicos
11.50 Manifestaciones de firma
(a) Signed electronic records shall contain information associated with the signing that clearly indicates all of the following:
(1) El nombre impreso del firmante;
(2) La fecha y hora en que se ejecutó la firma; y
(3) El significado (como revisión, aprobación, responsabilidad o autoría) asociado con la firma.
(b) Los elementos identificados en los párrafos (a) (1), (a) (2) y (a) (3) de esta sección estarán sujetos a los mismos controles que los registros electrónicos y se incluirán como parte de cualquier lectura humana. forma del registro electrónico (tal como visualización electrónica o impresión).
testo Saveris proporciona toda la funcionalidad necesaria.
Para ciertas acciones del usuario, el sistema requiere una firma electrónica. Esta firma también se muestra en el registro de auditoría con la especificación del motivo de la firma, por ejemplo, para cambiar la configuración. Una firma electrónica puede ser obligatoria para actividades definidas por el usuario, tales como:
- Alarmas de reconocimiento
- Cambiar la configuración de la alarma
- Editar configuración para informes automáticos
- Defina el contenido del informe y cree un informe único.
- Cambio de configuraciones en el rango del sistema.
- Editar la configuración de seguridad.
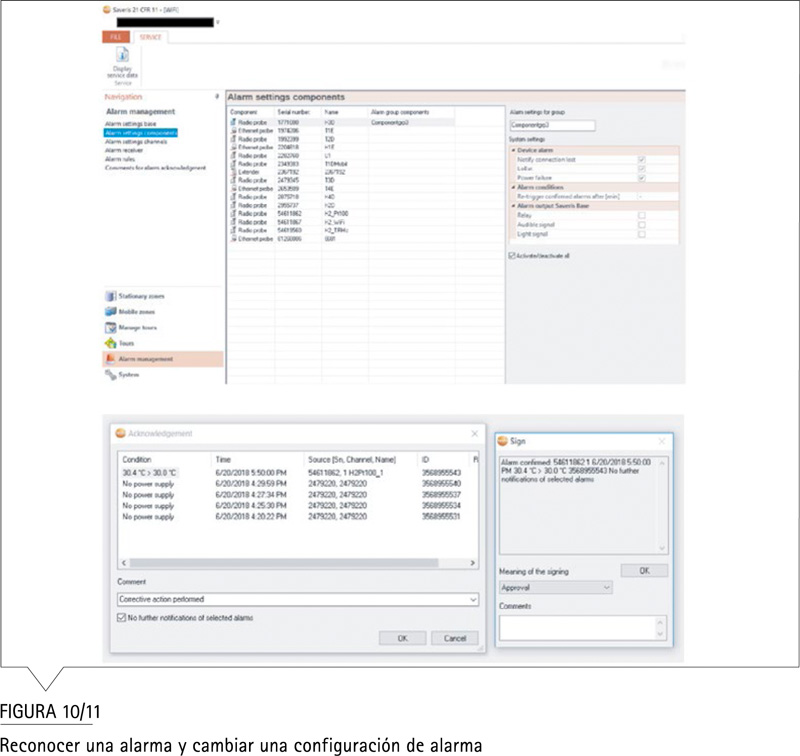
11.70 Firma / registro de enlaces
Las firmas electrónicas y las firmas manuscritas ejecutadas a registros electrónicos se vincularán a sus respectivos registros electrónicos para garantizar que las firmas no puedan ser eliminadas, copiadas o transferidas para falsificar un registro electrónico por medios ordinarios.
Datos de firma electrónica como parte integrante del registro.
Con testo Saveris, las firmas electrónicas una vez creadas ya no se pueden eliminar, copiar ni alterar utilizando métodos convencionales. Las firmas electrónicas podrían imponerse y configurarse para los siguientes parámetros / acciones:
- Edición y reconocimiento de alarmas.
- Definición del contenido de un informe.
- Cambiar la configuración del sistema
- Zonas de edición
- Ajustes de edición para informes automáticos
- Edición de control de acceso.
Para todas las acciones se puede hacer un comentario obligatorio.

Firmas electrónicas y controles
Requerimientos generales
(a) Cada firma electrónica será exclusiva de un individuo y no podrá ser reutilizada ni reasignada a ninguna otra persona.
(b) Antes de que una organización establezca, asigne, certifique o de otro modo sancione la firma electrónica de un individuo, o cualquier elemento de dicha firma electrónica, la organización debe verificar la identidad del individuo.
(c) Las personas que utilicen firmas electrónicas deberán, antes o en el momento de dicho uso, certificar ante la agencia que las firmas electrónicas en su sistema, utilizadas a partir del 20 de agosto de 1997, deben ser el equivalente legalmente vinculante de las firmas manuscritas tradicionales.
testo Saveris proporciona firmas electrónicas únicas.
En testo Saveris Pharma Solutions, la combinación de firma electrónica de cada persona es única. Las firmas electrónicas se implementan utilizando una combinación de un nombre de inicio de sesión único y una contraseña de firma. Una firma electrónica puede ser obligatoria para las actividades definidas del usuario.
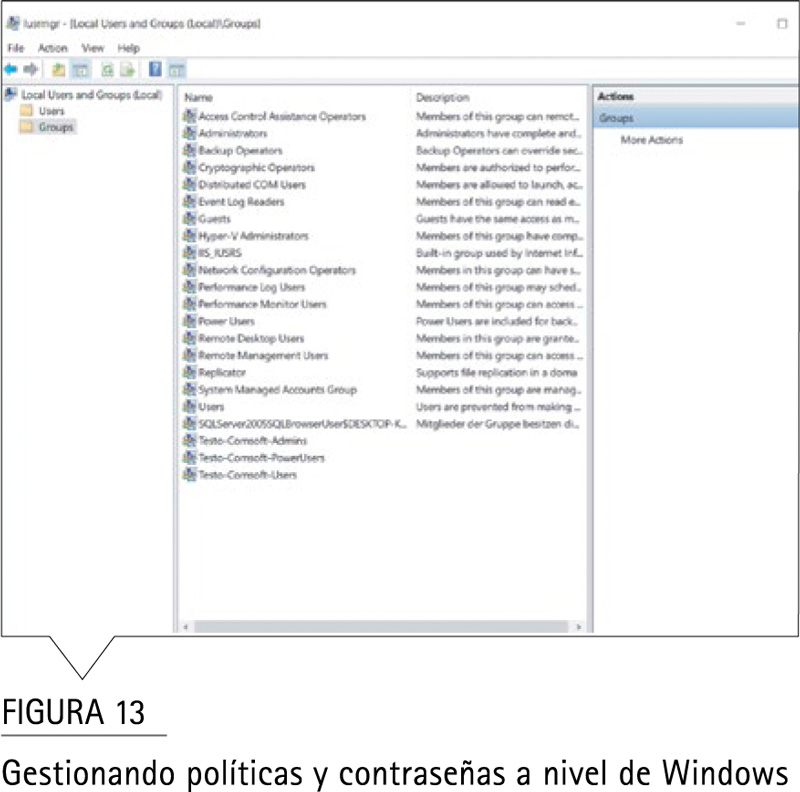
Firmas electrónicas no biométricas
Componentes y controles de firma electrónica.
(a) Las firmas electrónicas que no estén basadas en datos biométricos deberán:
(1) Utilice al menos dos componentes de identificación distintos, como un código de identificación y una contraseña.
(i) Cuando un individuo ejecuta una serie de firmas durante un período único y continuo de acceso controlado al sistema, la primera firma se ejecutará utilizando todos los componentes de la firma electrónica; las firmas posteriores se ejecutarán utilizando al menos un componente de firma electrónica que solo sea ejecutable y diseñado para ser utilizado por el individuo.
(ii) Cuando una persona ejecuta una o más firmas que no se realizan durante un período único y continuo de acceso controlado al sistema, cada firma se ejecutará utilizando todos los componentes de la firma electrónica.
(2) Ser usados sólo por sus dueños genuinos; y
(3) Ser administrado y ejecutado para garantizar que el intento de uso de la firma electrónica de un individuo por alguien que no sea su verdadero propietario requiera la colaboración de dos o más individuos.
(b) Las firmas electrónicas basadas en datos biométricos deben diseñarse para garantizar que no puedan ser utilizadas por nadie que no sea su verdadero propietario.
Máxima seguridad por la política de contraseña de Windows
Dado que nuestra solución es compatible con la firma electrónica de inicio de sesión LDAP está controlada por una política de contraseña segura de Windows. De acuerdo con las directrices de la FDA, testo Saveris emplea dos componentes de identificación: inicio de sesión y contraseña.
Regulaciones de seguridad correspondientes a la gestión de contraseñas
Controles para códigos de identificación / contraseñas
Las personas que utilizan firmas electrónicas basadas en el uso de códigos de identificación en combinación con contraseñas deben emplear controles para garantizar su seguridad e integridad. Dichos controles incluirán:
(a) Mantener la singularidad de cada código de identificación y contraseña combinados, de modo que no haya dos personas que tengan la misma combinación de código de identificación y contraseña.
(b) Asegurarse de que los códigos de identificación y las emisiones de contraseñas se verifiquen, recuperen o revisen periódicamente (por ejemplo, para cubrir eventos como la caducidad de las contraseñas).
(c) Seguir los procedimientos de gestión de pérdidas para desautorizar electrónicamente las fichas, tarjetas y otros dispositivos perdidos, robados, extraviados o potencialmente comprometidos que contengan o generen código de identificación o información de contraseña, y emitir reemplazos temporales o permanentes utilizando controles adecuados y rigurosos.
(d) El uso de salvaguardas de transacciones para evitar el uso no autorizado de contraseñas y / o códigos de identificación, y para detectar e informar de manera inmediata y urgente cualquier intento de uso no autorizado a la unidad de seguridad del sistema y, según corresponda, a la administración de la organización.
(e) Pruebas iniciales y periódicas de dispositivos, como fichas o tarjetas, que llevan o generan información de código de identificación o contraseña para garantizar que funcionan correctamente y no se han alterado de manera no autorizada.
Administración de contraseñas conveniente y segura
El software testo Saveris ayuda al administrador del sistema a crear y administrar contraseñas a través de controles integrados como la longitud de la contraseña y consultas como los límites de edad en el marco de la política de contraseñas de Windows. La administración de contraseñas garantizará nombres de usuario y contraseñas únicos para diferentes personas, así como el envejecimiento de las contraseñas y el bloqueo de cuentas después de intentos fallidos.
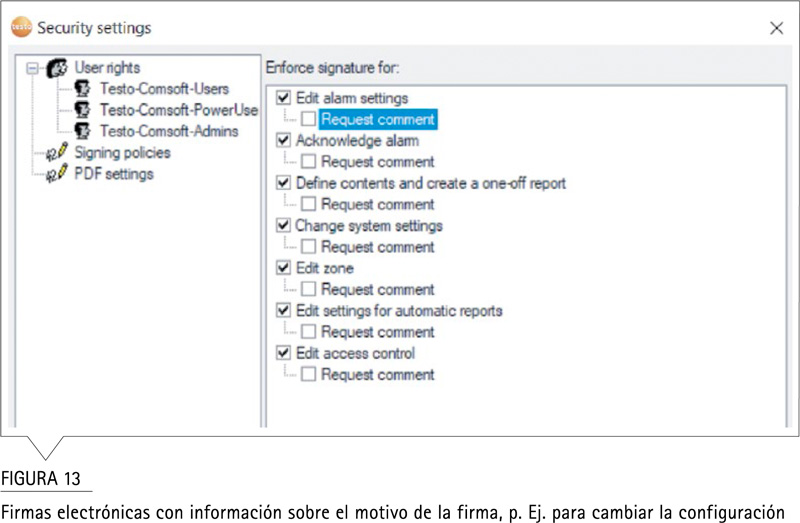
Del lado seguro: testo Saveris CFR
testo Saveris Pharma Solutions cumple los requerimientos de 21 CFR Parte 11
21 CFR Parte 11 regula la creación, el archivo y la gestión de la documentación electrónica, y sigue una estricta política de firma electrónica. Con el sistema testo Saveris completamente libre de papel, Testo ofrece la solución ideal para cumplir con todos los requisitos de CFR en términos de funcionalidad técnica.
Características relevantes del CFR de un vistazo:
- Sistema de monitorización de datos de medición testado con certificado del Fraunhofer IESE.
- Máxima integridad de datos proporcionada por estrictos protocolos de seguridad.
- Integración completa del concepto de acceso en el sistema de seguridad de Windows probado y probado
- Concepto de autorización
- Administración de contraseña / firma conveniente y segura
- Protocolo propio de Testo (propietario) con comunicación inalámbrica y ethernet.
- Almacenamiento de datos con base de datos verificada por suma de comprobación
- Uso de sumas de comprobación para garantizar la transmisión correcta y segura de los datos.
- Copia de seguridad diaria automática y copia de seguridad manual de archivos de base de datos posible
- Listo para una posible auditoría de la FDA en cualquier momento.
Nuestros clientes se benefician de los altos estándares de seguridad tecnológica proporcionados por el cumplimiento de CFR junto con un monitoreo de datos de medición altamente preciso y confiable en sus procesos farmacéuticos y médicos.
Servicios relacionados con testo Saveris CFR Pharma Solutions
Servicio de pre-instalación:
- Gestión de proyectos y asesoramiento personalizado.
- Mapeo térmico para la determinación óptima de la ubicación de la sonda
Servicios de calibración y calificación/validación
- El software de ajuste que utiliza las propias calibraciones / ajustes del cliente es posible (protección con contraseña, trazabilidad histórica de los datos de ajuste en el software testo Saveris CFR)
- Para los sistemas configurados con sondas digitales, los datos de calibración y fecha de caducidad se almacenan en la sonda
- Servicio de calibración en laboratorios y en sitio en numerosos países.
Calificación / validación:
Testo proporciona un conjunto completo de documentación y servicios relacionados con la instalación, puesta en servicio, calificación y validación de hardware y software para todas las soluciones de testo Saveris Pharma:
- DQ (Calificación de diseño), IQ (Calificación de instalación), OQ (Calificación operacional), PQ (Calificación de performance)
- Evaluación de riesgos personalizada según GAMP5.
Planes de mantenimiento y soporte adaptados a sus necesidades:
Plan de cuidado básico
Si solo necesita una configuración técnica y una prueba de funcionamiento del sistema de monitoreo con documentación compatible con GxP, encontrará la solución adecuada en nuestro plan de atención básica.
Plan Premium
El Plan Premium también te ofrece Un modelo basado en el riesgo. Con la validación completa de GAMP5, que puede incluir sus requisitos específicos para implementar el análisis de riesgos, después de lo cual puede pasar directamente al uso productivo. El proceso de análisis de riesgos modular y detallado. (FMEA) y la documentación coherente de calificación y validación facilita no solo la trazabilidad sino también la evaluación de futuras modificaciones del sistema, de forma rápida y segura.
Plan Peace of Mind
El plan Peace of Mind permite el máximo tiempo de actividad del sistema con gestión de recalibración y revalidación, así como gestión de repuestos y copias de seguridad si es necesario.
Más información en www.testo.com
[1] Para más información sobre FDA 21 CFR Parte 11, Además de la redacción original, visite los siguientes sitios web: http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch. cfm?CFRPart=11Guidance for Industry1 Part 11, Electronic Records;
Electronic Signatures – Scope and Application http://www.fda.gov/RegulatoryInformation/Guidances/ucm125067.htm http://www.fda.gov/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm124787.htm
[2] 2 Para AWS y GxP, visite https://d1.awsstatic.com/whitepapers/compliance/Using_AWS_in_GxP_Systems.pdf
[3] El cifrado predeterminado de Amazon S3 proporciona una manera de establecer el comportamiento de cifrado predeterminado para un grupo de S3. Puede establecer el cifrado predeterminado en un contenedor para que todos los objetos se cifren cuando se almacenan en el contenedor. Los objetos se cifran utilizando el cifrado del lado del servidor con claves administradas de Amazon S3 (SSE-S3) o claves administradas de AWS KMS (SSE-KMS). Referencia:https://docs.aws.amazon.com/AmazonS3/latest/dev/bucket-encryption.html
Más información:
info@testo.com.ar
www.testo.com.ar