
Equipos para la determinación de Nitrógeno

El NITRÓGENO es un elemento muy demandado por los vegetales, por lo que es un constituyente de las proteínas, el nitrógeno desempeña un papel fundamental en el metabolismo vegetal. Es esencial para la estructura y funciones en las células y para todas las reacciones enzimáticas, además de hacer parte de la molécula de la clorofila (fotosíntesis) y ser un componente de las vitaminas.
El nitrógeno es uno de los componentes químicos de las proteínas, que desempeñan un papel importante en nuestro organismo, al proporcionar materiales para la construcción y para el mantenimiento de todos los órganos y tejidos, y por participar en la formación de hormonas, enzimas y anticuerpos.
DETERMINACIÓN DE PROTEÍNAS
La determinación de proteínas en una muestra es basada en la determinación de nitrógeno, realizada en sectores como:
ALIMENTOS: Los niveles de proteínas deben estar adecuados en los alimentos para una dieta balanceada. Las proteínas tienen propiedades importantes funcionales en el propio alimento, como características de textura.
AMBIENTAL: Se verifican los niveles de proteínas en hojas y granos. Por ejemplo: la calidad de granos de cebada para la producción de malta es perjudicada cuando el contenido de proteínas en el grano sobrepasa el índice de 12%.
SUELOS: El nitrógeno en el suelo se encuentra principalmente en forma orgánica. El nitrógeno orgánico es transformado en amoníaco, que es oxidado para nitrato, un buen indicador de la actividad biológica y de la fertilidad del suelo.
AUTOMOVILÍSTICO: Para determinar compuestos orgánicos volátiles de materiales como tejido, plástico y caucho. Poseen alta presión de vapor, lo que hace con que se transformen en gas al entrar en contacto con la atmosfera, generando el conocido “olor de carro nuevo”, tan apreciado por los clientes.
DETERMINACIÓN DE NITRÓGENO
Para la determinación de nitrógeno, fueron desarrollados métodos como:
DUMAS: Primer método descrito para el análisis de nitrógeno y proteína, realizado por medio de la utilización de temperaturas elevadas, llevando a la oxidación total de la muestra en presencia de oxigeno y a la inmediata reducción de los óxidos de nitrógeno y la consecuente detección del nitrógeno molecular producido. Este método puede presentar divergencias en sus resultados, debido a la baja cantidad de la muestra utilizada.
LUMINISCENCIA: Fenómeno caracterizado por la emisión de luz de una molécula que estaba en su estado excitado. Existen tres tipos de luminiscencia que son utilizadas en análisis de gases: la fotoluminiscencia, normalmente conocida como fluorescencia, la quimioluminiscencia y la fotometría de llama. Un factor que puede dificultar el análisis en la quimioluminiscencia es la presencia de interferentes.
KJELDHAL: Se fundamenta en la destrucción de la materia orgánica con ácido sulfúrico concentrado, en presencia de un catalizador con acción de calor, con posterior destilación y titulación del nitrógeno proveniente de la muestra. Ventajas: sencillo, preciso, bajo costo, modificado para análisis de microgramos de proteína (micro Kjeldhal). Método en que son utilizadas mayores cantidades de muestra y, así, presenta menor chance de errores.
MUESTREO, PREPARACIÓN Y SOLUBILIZACIÓN
Además de la mejor selección del método analítico, son fundamentales un buen muestreo, preparación y solubilización de la muestra para el análisis. El muestreo es la primera fase del análisis y, en algunos casos, es necesario reducir considerablemente la dimensión de la muestra antes que esta sea introducida en el sistema analítico.
El método de preparación utilizado dependerá del tipo de muestra, sin embargo, siempre el material colectado debe ser preparado en un local apropiado y equipado para esta finalidad. Normalmente, la actividad de preparación incluye: recibimiento, registro, pre-acondicionamiento, secado, molienda, acondicionamiento y rotulado de las muestras.
RECOMENDACIÓN: Escoger el molino adecuado para la molienda de la muestra sólida, que sigue para la determinación de proteína, es fundamental. Es necesario estar atento, para que no ocurra el calentamiento de la muestra, lo que posibilitaría una desnaturalización de las proteínas, lo que influenciaría directamente en los resultados finales del análisis
MÉTODO KJELDHAL
El método más tradicional de determinación de nitrógeno fue desarrollado hace más de 130 anos por el dinamarqués Johan Kjeldahl, que estudiaba proteínas en granos. Titulado como Método Kjeldahl, es ampliamente utilizado en la determinación de nitrógeno total, que, indirectamente, posibilita la determinación de la proteína bruta. A pesar de algunos cambios a lo largo de los años, la esencia de la metodología permanece la misma hasta los días actuales.
El método Kjeldahl está presente en diversas normas oficiales, como AOAC, Standard Methods for the Examination of Water and Waste water, entre otras. Tales normas aseguran características como calidad, seguridad, confiabilidad y eficiencia.
APLICACIÓN DEL MÉTODO KJELDAHL
Para que el Método Kjeldahl sea aplicado, son necesarios equipos de fácil manipulación y algunos accesorios para la obtención del resultado buscado:
BALANZA ANALÍTICA: Utilizada en el peso de la muestra antes de ser colocada en el tubo de vidrio en borosilicato, que seguirá para el bloque digestor. Proporciona datos exactos y específicos en relación al peso.
MOLINO: Para la desintegración de la muestra. Permite el aumento de la superficie de contacto y, consecuentemente, la mejora en la eficiencia de las etapas sucesivas de preparo, además de la uniformidad en el tamaño de las partículas. Ayuda en la mejor homogeneización de la muestra y también de la mejor separación del componente a ser analizado.
TUBO DE BOROSILICATO: Local donde la muestra será colocada junto al ácido concentrado y catalizadores, para que sea llevada al bloque digestor. Es un tipo de vidrio resistente al calor y a los elementos químicos. Es posible utilizar tubos micro o macro, dependiendo de la necesidad. Para muestras en que hay menor cantidad de nitrógeno, cantidades mayores son necesarias y, consecuentemente, se utiliza un tubo macro. Para muestras en que hay mayor cantidad de nitrógeno, cantidades menores son necesarias y de esta forma, se utilizan tubos micro.
BLOQUE DIGESTOR: Donde será realizada la digestión de la muestra. Se trata de una especie de cámara, con funcionamiento semejante a una placa calentadora. Sin embargo, hay encajes para la colocación de tubos con las muestras. (Conozca más sobre Bloques Digestores de Tecnal en los Cuadros 1 y 2)


CÁMARA DE EXTRACCIÓN O SISTEMA DE EXTRACCIÓN
Como la reacción es por medio de ácido concentrado, el bloque digestor debe ser colocado dentro de una cámara extractora, para que los gases sean liberados durante el proceso de digestión. La cámara puede ser substituida por un sistema de extracción (galería extractora, scrubber y garrafa neutralizadora). La galería extractora es encajada en el bloque digestor, arriba de los tubos, y es conectada a un scrubber, responsable por la succión de los gases, neutralizados en la garrafa. (Conozca más sobre cámaras y sistemas de extracción Tecnal en los Cuadros 3, 4, 5 y 6)




DESTILADOR DE NITRÓGENO
Responsable por la destilación de la muestra previamente digerida en el bloque digestor. (Conozca más sobre el destilador de nitrógeno Tecnal en cuadro 7)

APLICACIÓN DEL MÉTODO KJELDAHL
RECOMENDACIÓN: El destilador de nitrógeno, TE-0364-Tecnal posee entradas de agua independientes para la caldera y el condensador. De esta forma, es posible utilizar un baño termostático, TE-2005-Tecnal para enfriamiento del condensador, lo que proporciona gran economía de agua.
ERLENMEYER: Colocado en la salida del condensador del destilador de nitrógeno, para colectar el destilado que será sometido a la titulación.
BURETA: Será titulado un ácido al destilado.
La bureta de vidrio está sujeta al daño y a errores de lectura por el usuario. Puede ser substituida por una bureta digital, que coloca la dosis correcta de determinado volumen.
ETAPAS DEL MÉTODO KJELDAHL
El método es dividido en tres principales etapas: digestión, destilación y titulación.
DIGESTIÓN
La muestra ya homogeneizada (después de molida) que seguirá para la digestión es previamente pesada en la balanza analítica y mezclada en la proporción necesaria de ácido sulfúrico concentrado en un tubo en borosilicato. Es adicionado catalizador que actuará en la aceleración de la digestión.
Los catalizadores normalmente utilizados son:
BLOQUE DIGESTOR: Para que la muestra y el ácido sulfúrico reacciones de manera efectiva.
SELENITO DE SODIO: Para minimizar detonaciones dentro del tubo.
SULFATO DE SODIO: Para elevar el punto de ebullición del ácido sulfúrico para aproximadamente 360°C.
RECOMENDACIÓN: Cuando la muestra sea muy grasosa, es posible utilizar un antiespumante durante la digestión.
La mezcla preparada es colocada en el bloque digestor. La temperatura mínima del bloque para que la reacción ocurras es de 350°C, sin embargo, normalmente, es fijada en 400°C, para garantizar la eficiencia del proceso. Con el calentamiento del bloque digestor juntamente con la mezcla ácida, el carbono contenido en la muestra es oxidado, el dióxido de carbono se desprende y el nitrógeno es transformado en sulfato de amonio, transformando la muestra oscura en una solución translúcida, normalmente, verde clara. En este momento, la digestión es finalizada.
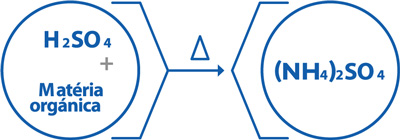
Esa etapa produce gases tóxicos, entonces debe ser realizada en cámara de extracción o, si es necesario, utilizar el sistema de extracción y neutralización de gases.
RECOMENDACIÓN: El bloque digestor, TE-040/25-Micro o TE-008/50-04-Macro – Tecnal posee el controlador separado, que puede permanecer fuera de la cámara de extracción, lo que evita posibles daños causados por la reacción ácida del proceso de digestión y aumenta la vida útil del equipo.
DESTILACIÓN
Después de la digestión de la muestra, la solución de sulfato de amonio obtenida en el tubo es enfriada a temperatura ambiente y, posteriormente, es llevada al destilador de nitrógeno. Antes de comenzar la destilación. Es necesario que sea colocado un Erlenmeyer en la salida del condensador del equipo, que deberá contener ácido bórico y un indicador, generalmente, rojo de metilo.
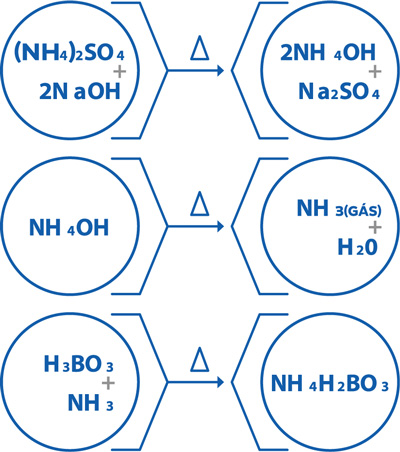
El tubo de borosilicato es colocado en el destilador, donde es dosificado hidróxido de sodio para la neutralización. El sulfato de amonio, presente en el tubo, en contacto con el hidróxido de sodio dosificado y el vapor de agua de la caldera del equipo, es transformado en hidróxido de amonio y, así, liberado en estado gaseoso.
Cuando el hidróxido de amonio es liberado, éste pasa por el sistema de destilación del equipo y condensa dentro del Erlenmeyer que fue preparado previamente con ácido bórico y el indicador, formando el borato de amonio en una coloración que pasa de rojo pálido para verde. De esta forma, es finalizada la destilación de la muestra.
En esta de la destilación, la utilización en conjunto del destilador con un baño termostático reduce considerablemente el consumo de agua para enfriar el condensador.
TITULACIÓN DETERMINACIÓN
En la etapa de titulación, es colocado en una bureta, normalmente, ácido clorhídrico y un indicador, verde de bromocresol o azul de bromotimol, que son titulados en el borato de amonio, que fue formado en la etapa de destilación.
El ácido clorhídrico es titulado hasta que alcance el punto de cambio del destilado, lo que altera su coloración para incolora/gris. Cuando esa coloración es identificada, la titulación está finalizada.
Después de finalizar la titulación, la proteína bruta es mensurada por medio del cálculo:
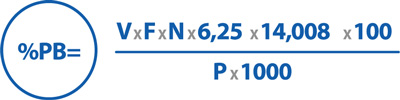
V: Volumen de la solución de ácido clorhídrico usado para titular la muestra – Volumen de la solución de ácido clorhídrico usado para titular el blanco.
F: Factor de la solución de ácido clorhídrico.
N: Normalidad de la solución de ácido clorhídrico
6,25: Factor de transformación de nitrógeno en proteína bruta
14,008: Equivalente en gramo de nitrógeno
P: Peso de la muestra
*En el caso de alimentos, de acuerdo con el tipo de muestra, el factor de conversión varia de 3,24 la 6,26.
CONCLUSIÓN
El método Kjeldahl es uno de los más utilizados para la determinación de nitrógeno en substancias orgánicas y se mantiene como un procedimiento directo y sencillo. Se trata de un método más tradicional, en el que son utilizadas mayores cantidades de muestra, lo que posibilita menor chance de errores.
Así, los mejores resultados serán obtenidos por medio del uso de esa metodología, asociada a la utilización de los equipos de Tecnal, empresa reconocida por invertir en investigación y tecnología, lo que posibilita equipos de calidad y la obtención de resultados más seguros.














